
½šŹōĪŁÓĆĶ¾¹ć·ŗ£¬Ö÷ŅŖÓĆÓŚÖĘŌģÓ²ÖŹ»ņÄĶøßĪĀµÄŗĻ½š£¬ŅŌ¼°µĘÅŻµÄµĘĖ攣øßĪĀĻĀ£¬ŌŚĆܱÕČŻĘ÷ÖŠÓĆH2»¹ŌWO3æɵƵ½½šŹōĪŁ£¬Ęä×Ü·“Ó¦ĪŖ£ŗ
WO3 (s) + 3H2 (g) W (s) + 3H2O (g)
W (s) + 3H2O (g)
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ÅÉĻŹö·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖ___________________________”£
¢ĘijĪĀ¶ČĻĀ·“Ó¦“ļĘ½ŗāŹ±£¬H2ÓėĖ®ÕōĘųµÄĢå»ż±ČĪŖ2:3£¬ŌņH2µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ_____________________£»ĖęĪĀ¶ČµÄÉżøߣ¬H2ÓėĖ®ÕōĘųµÄĢå»ż±Č¼õŠ”£¬ŌņøĆ·“Ó¦ĪŖ·“Ó¦_____________________£ØĢī”°ĪüČČ”±»ņ”°·ÅČČ”±£©”£
¢ĒÉĻŹö×Ü·“Ó¦¹ż³Ģ“óÖĀ·ÖĪŖČżøö½×¶Ī£¬ø÷½×¶ĪÖ÷ŅŖ³É·ÖÓėĪĀ¶ČµÄ¹ŲĻµČēĻĀ±ķĖłŹ¾£ŗ
| ĪĀ¶Č | 25”ę ~ 550”ę ~ 600”ę ~ 700”ę |
| Ö÷ŅŖ³É·Ż | WO3 W2O5 WO2 W |
 W (s) + 2H2O (g)£»¦¤H £½ +66.0 kJ”¤mol£1
W (s) + 2H2O (g)£»¦¤H £½ +66.0 kJ”¤mol£1  W (s) + 2H2O (g)£»¦¤H £½ £137.9 kJ”¤mol£1
W (s) + 2H2O (g)£»¦¤H £½ £137.9 kJ”¤mol£1  WO2 (g) µÄ¦¤H £½ ______________________”£
WO2 (g) µÄ¦¤H £½ ______________________”£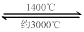 WI4 (g)”£ĻĀĮŠĖµ·ØÕżČ·µÄÓŠ____________”£
WI4 (g)”£ĻĀĮŠĖµ·ØÕżČ·µÄÓŠ____________”££Ø1£© £Ø2£©60% ĪüČČ
£Ø2£©60% ĪüČČ
£Ø3£©2WO3+H2=W2O5+H2O£» W2O5ŗĶWO2”¢ 1:1:4£»
£Ø4£©+203.9KJ.mol-1 £Ø5£© a”¢b”£
½āĪöŹŌĢā·ÖĪö£ŗ
£Ø1£©øł¾Ż·½³ĢŹ½æɵƔ£
£Ø2£©H2ÓėĖ®ÕōĘųµÄĢå»ż±Č¼õŠ”£¬ĖµĆ÷·“Ó¦ÕżĻņŅĘ¶Æ£¬ŌņÕż·“Ó¦ŹĒĪüČČ·“Ó¦”£
£Ø3£©ÓɱķøńŠÅĻ¢æÉÖŖ£¬µŚŅ»½×¶Ī·“Ó¦Ź±£ŗ2WO3+H2=W2O5+H2O£¬Ö÷ŅŖ³É·ÖĪŖ£ŗW2O5ŗĶWO2”£
£Ø4£©øł¾ŻøĒĖ¹¶ØĀÉ£¬¦¤H £½+203.9 KJ.mol-1
£Ø5£©a”¢µāµ„ÖŹŅ×Éż»Ŗ£¬æÉŅŌÖŲø“Ź¹ÓĆ”£
b”¢WI4ŌŚµĘĖæÉĻ·Ö½āŗóæÉŅŌÖŲŠĀ³Įµķ”£
æ¼µć£ŗæ¼²éĮĖ»ÆŃ§Ę½ŗā³£Źż£¬»Æѧ·“Ó¦ČČ£¬»ÆŃ§Ę½ŗāŅĘ¶ÆµČÖŖŹ¶”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©ŌŚ298KŹ±£¬1molCH4ŌŚŃõĘųÖŠĶźČ«Č¼ÉÕÉś³É¶žŃõ»ÆĢ¼ŗĶŅŗĢ¬Ė®£¬·Å³öČČĮæ890.0 kJ”£Š“³öøĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ ”£ĻÖÓŠCH4ŗĶCOµÄ»ģŗĻĘųĢå0.75mol£¬ĶźČ«Č¼ÉÕŗó£¬Éś³ÉCO2ĘųĢåŗĶ18æĖŅŗĢ¬Ė®£¬²¢·Å³ö515kJČČĮ棬ŌņCH4ŗĶCOµÄĪļÖŹµÄĮæ·Ö±šĪŖ ”¢ mol.
£Ø2£©ĄūÓĆøĆ·“Ó¦Éč¼ĘŅ»øöČ¼ĮĻµē³Ų£ŗÓĆĒāŃõ»Æ¼ŲČÜŅŗ×÷µē½āÖŹČÜŅŗ£¬¶ąæ׏ÆÄ«×öµē¼«£¬ŌŚµē¼«ÉĻ·Ö±šĶØČė¼×ĶéŗĶŃõĘų”£ĶØČė¼×ĶéĘųĢåµÄµē¼«Ó¦ĪŖ ¼«£ØĢīŠ“”°Õż”±»ņ”°øŗ”±£©£¬øƵē¼«ÉĻ·¢ÉśµÄµē¼«·“Ó¦ŹĒ £ØĢī×ÖÄø“śŗÅ£©”£
a. CH4”Ŗe- + 2O2 ="=" CO2 + 2H2O
b. CH4”Ŗ8e- + 10OH- ="=" CO32- + 7H2O
c. O2 + 2H2O + 4 e- ="=" 4OH-
d. O2”Ŗ4 e- + 4H+ ="=" 2H2O
£Ø3£©ŌŚČēĶ¼ĖłŹ¾ŹµŃé×°ÖĆÖŠ£¬ŹÆÄ«°ōÉĻµÄµē¼«·“Ó¦Ź½ĪŖ £»Čē¹ūĘšŹ¼Ź±Ź¢ÓŠ1000mL pH=5µÄĮņĖįĶČÜŅŗ£Ø25”ę£¬CuSO4×ćĮ棩£¬Ņ»¶ĪŹ±¼äŗóČÜŅŗµÄpH±äĪŖ1£¬“ĖŹ±æɹŪ²ģµ½µÄĻÖĻóŹĒ £»ČōŅŖŹ¹ČÜŅŗ»Öø“µ½ĘšŹ¼ÅØ¶Č£ØĪĀ¶Č²»±ä£¬ŗöĀŌČÜŅŗĢå»żµÄ±ä»Æ£©£¬æÉĻņČÜŅŗÖŠ¼ÓČė £ØĢīĪļÖŹĆū³Ę£©£¬ĘäÖŹĮæŌ¼ĪŖ ”£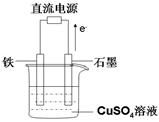
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
°ŃĆŗ×÷ĪŖČ¼ĮĻæÉĶعżĻĀĮŠĮ½ÖÖĶ¾¾¶£ŗ
Ķ¾¾¶I£ŗC(s) +O2 (g) == CO2(g) ”÷H1<0 ¢Ł
Ķ¾¾¶II£ŗĻČÖĘ³ÉĖ®ĆŗĘų£ŗC(s) +H2O(g) == CO(g)+H2(g) ”÷H2>0 ¢Ś
ŌŁČ¼ÉÕĖ®ĆŗĘų£ŗ2CO(g)+O2 (g) == 2CO2(g) ”÷H3<0 ¢Ū
2H2(g)+O2 (g) == 2H2O(g) ”÷H4<0 ¢Ü
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£© Ķ¾¾¶I·Å³öµÄČČĮæ ( Ģī”°“óÓŚ”±”°µČÓŚ”±»ņ”°Š”ÓŚ”±) Ķ¾¾¶II·Å³öµÄČČĮ攣
£Ø2£© ”÷H1”¢”÷H2”¢”÷H3”¢”÷H4µÄŹżŃ§¹ŲĻµŹ½ŹĒ ”£
£Ø3£©12gĢæ·ŪŌŚŃõĘųÖŠ²»ĶźČ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼£¬·Å³ö110£®35kJČČĮ攣ĘäČČ»Æѧ·½³ĢŹ½ĪŖ ”£
£Ø4£©ĆŗĢæ×÷ĪŖČ¼ĮĻ²ÉÓĆĶ¾¾¶IIµÄÓŵćÓŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŃŠ¾æNO2”¢SO2 ”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ²āĮæ¼°“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ唣
£Ø1£©I2O5æÉŹ¹H2S”¢CO”¢HC1µČŃõ»Æ£¬³£ÓĆÓŚ¶ØĮæ²ā¶ØCOµÄŗ¬Į攣ŅŃÖŖ£ŗ
2I2(s)+5O2(g)£½2I2O5(s) ”÷H£½£75.56 kJ”¤mol£1
2CO(g)+O2(g)£½2CO2(g) ”÷H£½£566.0 kJ”¤mol£1
Š“³öCO(g)ÓėI2O5(s)·“Ӧɜ³ÉI2(s)ŗĶCO2(g)µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø2£©Ņ»¶ØĢõ¼žĻĀ£¬NO2ÓėSO2·“Ӧɜ³ÉSO3ŗĶNOĮ½ÖÖĘųĢå£ŗNO2(g)+SO2(g) SO3(g)+NO(g)½«Ģå»ż±ČĪŖ1”Ć2µÄNO2”¢SO2ĘųĢåÖĆÓŚĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ĻĀĮŠÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ ”£
SO3(g)+NO(g)½«Ģå»ż±ČĪŖ1”Ć2µÄNO2”¢SO2ĘųĢåÖĆÓŚĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ĻĀĮŠÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ ”£
a£®ĢåĻµŃ¹Ēæ±£³Ö²»±ä
b£®»ģŗĻĘųĢåŃÕÉ«±£³Ö²»±ä
c£®SO3ŗĶNOµÄĢå»ż±Č±£³Ö²»±ä
d£®ĆæĻūŗÄ1molSO2µÄĶ¬Ź±Éś³É1molNO
²āµĆÉĻŹö·“Ó¦Ę½ŗāŹ±NO2ÓėSO2Ģå»ż±ČĪŖ1”Ć6£¬ŌņĘ½ŗā³£ŹżK£½ ”£
£Ø3£©“ÓĶŃĻõ”¢ĶŃĮņŗóµÄŃĢĘųÖŠ»ńČ”¶žŃõ»ÆĢ¼£¬ÓƶžŃõ»ÆĢ¼ŗĻ³É¼×“¼ŹĒĢ¼¼õÅŵĊĀ·½Ļņ”£½«CO2×Ŗ»ÆĪŖ¼×“¼µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO2 (g)£«3H2(g) CH3OH(g)£«H2O(g) ”÷H3
CH3OH(g)£«H2O(g) ”÷H3
¢ŁČ”Īå·ŻµČĢåĢå»żCO2ŗĶH2µÄµÄ»ģŗĻĘųĢå £ØĪļÖŹµÄĮæÖ®±Č¾łĪŖ1£ŗ3£©£¬·Ö±š¼ÓČėĪĀ¶Č²»Ķ¬”¢ČŻ»żĻąĶ¬µÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśÉĻŹö·“Ó¦£¬·“Ó¦ĻąĶ¬Ź±¼äŗ󣬲āµĆ¼×“¼µÄĢå»ż·ÖŹż¦Õ(CH3OH) Óė·“Ó¦ĪĀ¶ČTµÄ¹ŲĻµĒśĻßČēĶ¼ĖłŹ¾£¬ŌņÉĻŹöCO2×Ŗ»ÆĪŖ¼×“¼·“Ó¦µÄ”÷H3 0£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©”£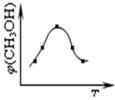
¢ŚŌŚČŻ»żĪŖ1LµÄŗćĪĀĆܱÕČŻĘ÷ÖŠ³äČė1molCO2ŗĶ3molH2£¬½ųŠŠÉĻŹö·“Ó¦”£²āµĆCO2ŗĶCH3OH(g)µÄÅضČĖꏱ¼ä±ä»ÆČēĻĀ×óĶ¼ĖłŹ¾”£ČōŌŚÉĻŹöĘ½ŗāĢåĻµÖŠŌŁ³ä0.5molCO2ŗĶ1.5molĖ®ÕōĘų£Ø±£³ÖĪĀ¶Č²»±ä£©£¬Ōņ“ĖĘ½ŗā½« ŅĘ¶Æ£ØĢī”°ĻņÕż·“Ó¦·½Ļņ”±”¢”°²»”±»ņ”°Äę·“Ó¦·½Ļņ”±£©”£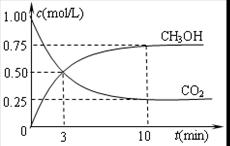
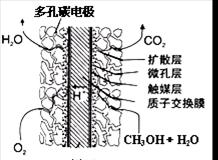
¢ŪÖ±½Ó¼×“¼Č¼ĮĻµē³Ų½į¹¹ČēÉĻÓŅĶ¼ĖłŹ¾”£Ę乤×÷Ź±øŗ¼«µē¼«·“Ó¦Ź½æɱķŹ¾ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
(1)CH4(g )+2O2(g )=CO2(g )+2H2O(g ) ¦¤H=-802.3kJ/mol
øĆČČ»Æѧ·“Ó¦·½³ĢŹ½µÄŅāŅåŹĒ_____________________________________”£
(2)ŅŃÖŖ2gŅŅ“¼ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®·Å³öQ kJµÄČČĮ棬Š“³ö±ķŹ¾ŅŅ“¼Č¼ÉÕČȵÄČČ»Æѧ·½
³ĢŹ½£ŗ____________________________________________________________.
(3)ŅŃÖŖ²šæŖ1mol H-H¼ü£¬1mol N-H¼ü£¬1mol 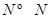 ¼ü·Ö±šŠčŅŖµÄÄÜĮæŹĒ436kJ”¢391KJ”¢946kJ£¬ŌņN2ÓėH2·“Ӧɜ³É1mol NH3(g)µÄČČ»Æѧ·½³ĢŹ½ŹĒ___________________.
¼ü·Ö±šŠčŅŖµÄÄÜĮæŹĒ436kJ”¢391KJ”¢946kJ£¬ŌņN2ÓėH2·“Ӧɜ³É1mol NH3(g)µÄČČ»Æѧ·½³ĢŹ½ŹĒ___________________.
(4)ŅĄ¾ŻøĒĖ¹¶ØĀÉæÉŅŌ¶ŌijŠ©ÄŃŅŌĶعżŹµŃéÖ±½Ó²ā¶ØµÄ»Æѧ·“Ó¦µÄģŹ±ä½ųŠŠĶĘĖć”£
ŅŃÖŖ£ŗC(ŹÆÄ«£¬s)+O2(g)=CO2(g) ¦¤H=-393.5kJ/mol ¢Ł
2H2(g)+O2(g)=2H2O(l) ¦¤H=-571.6kJ/mol ¢Ś
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ¦¤H=-2599kJ/mol ¢Ū
øł¾ŻøĒĖ¹¶ØĀÉ£¬¼ĘĖć298KŹ±ÓÉC£ØŹÆÄ«£¬s£©ŗĶH2(g)Éś³É1mol C2H2(g)·“Ó¦µÄģŹ±ä£ŗ
____________________________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ÓĆ”°£¾”±”¢”°£¼”±»ņ”°£½”±ĢīæÕ£ŗ
£Ø1£©Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬H2(g)+Cl2(g)£½2HCl(g)£¬¹āÕÕŗĶµćČ¼Ģõ¼žµÄ¦¤H£Ø»Æѧ¼ĘĮæŹżĻąĶ¬£©·Ö±šĪŖ¦¤H1”¢¦¤H2£¬¦¤H1______¦¤H2£»
£Ø2£©ĻąĶ¬Ģõ¼žĻĀ£¬2molĒāŌ×ÓĖł¾ßÓŠµÄÄÜĮæ 1molĒā·Ö×ÓĖł¾ßÓŠµÄÄÜĮ棻
£Ø3£©ŅŃÖŖ³£ĪĀŹ±ŗģĮױȰ×Į×ĪČ¶Ø£¬±Č½ĻĻĀĮŠ·“Ó¦ÖŠ¦¤HµÄ“󊔣ŗ¦¤H1_____¦¤H2”£
¢Ł4P(°×Į×£¬s) +5O2(g)£½2P2O5(s) ¦¤H1£¬¢Ś4P(ŗģĮ×£¬s)+5O2(g)£½2P2O5(s) ¦¤H2£»
£Ø4£©ŅŃÖŖ£ŗ101 kPaŹ±£¬2C(s) +O2(g)£½2CO(g) ¦¤H£½£221kJ”¤mol£1£¬ŌņĢ¼µÄČ¼ÉÕČČŹżÖµ 110.5 kJ”¤mol£1£»
£Ø5£©ŅŃÖŖ£ŗĻ”ČÜŅŗÖŠ£¬H£«(aq)+OH£ (aq)£½H2O(l) ¦¤H£½£57.3kJ/mol£¬ŌņÅØĮņĖįÓėĻ”NaOHČÜŅŗ·“Ӧɜ³É1 molĖ®£¬·Å³öµÄČČĮæ 57.3 kJ£»
£Ø6£©æÉÄę·“Ó¦£ŗaA(Ęų)+bB(Ęų) cC(Ęų)+dD(Ęų)£»¦¤H£½Q£¬øł¾ŻĶ¼»Ų“š£ŗ
cC(Ęų)+dD(Ęų)£»¦¤H£½Q£¬øł¾ŻĶ¼»Ų“š£ŗ
P1 ______ P2£»¢Ś£Øa+b£©______£Øc+d£©£»¢Ūt1”ę______ t2”ę”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
(14·Ö)2014Äź10ŌĀ³õ£¬Īķö²ĢģĘų¶ą“ĪĖĮÅ°ŗÓ±±”¢Ģģ½ņ”¢±±¾©µČµŲĒų”£ĘäÖŠ£¬Č¼ĆŗŗĶĘū³µĪ²ĘųŹĒŌģ³ÉæÕĘųĪŪČ¾µÄŌŅņÖ®Ņ»”£
£Ø1£©Ęū³µĪ²Ęų¾»»ÆµÄÖ÷ŅŖŌĄķĪŖ£ŗ2NO(g) + 2CO(g) 2CO2(g)+ N2(g)”£”÷H£¼0
2CO2(g)+ N2(g)”£”÷H£¼0
¢ŁøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ ”£
¢ŚČōøĆ·“Ó¦ŌŚ¾ųČČ”¢ŗćČŻµÄĆܱÕĢåĻµÖŠ½ųŠŠ£¬ĻĀĮŠŹ¾ŅāĶ¼ÕżČ·ĒŅÄÜĖµĆ÷·“Ó¦ŌŚ½ųŠŠµ½t1Ź±æĢ“ļµ½Ę½ŗāדĢ¬µÄŹĒ £ØĢī“śŗÅ£©”£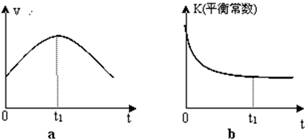
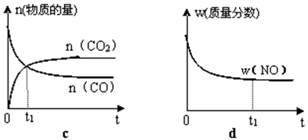
£Ø2£©Ö±½ÓÅÅ·ÅĆŗČ¼ÉÕ²śÉśµÄŃĢĘų»įŅżĘšŃĻÖŲµÄ»·¾³ĪŹĢā”£ĆŗČ¼ÉÕ²śÉśµÄŃĢĘųŗ¬µŖµÄŃõ»ÆĪļ£¬ÓĆCH4“߻ƻ¹ŌNOxæÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£
ŅŃÖŖ£ŗCH4(g)+2NO2(g)£½N2(g)£«CO2(g)+2H2O(g) ”÷H£½£867 kJ/mol
2NO2(g)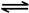 N2O4(g) ”÷H£½£56.9 kJ/mol
N2O4(g) ”÷H£½£56.9 kJ/mol
H2O(g) £½ H2O(l) ¦¤H £½ £44.0 kJ£Æmol
Š“³öCH4“߻ƻ¹ŌN2O4(g)Éś³ÉN2ŗĶH2O(l)µÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
£Ø3£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬Ņ²æÉŅŌÓĆNH3“¦ĄķNOx”£ŅŃÖŖNOÓėNH3·¢Éś·“Ӧɜ³ÉN2ŗĶH2O£¬ĻÖÓŠNOŗĶNH3µÄ»ģŗĻĪļ1mol£¬³ä·Ö·“Ó¦ŗóµĆµ½µÄ»¹Ō²śĪļ±ČŃõ»Æ²śĪļ¶ą1.4 g£¬ŌņŌ·“Ó¦»ģŗĻĪļÖŠNOµÄĪļÖŹµÄĮææÉÄÜŹĒ_____________”£
£Ø4£©ŅŌ¼×ĶéĪŖŌĮĻÖĘČ”ĒāĘųŹĒ¹¤ŅµÉĻ³£ÓƵÄÖĘĒā·½·Ø”£Ōņ2 molCH4Óė×ćĮæH2O£Øg£©·“Ó¦×ī¶ąæÉÉś³É_______mol H2£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½_________________________________________________”£
(5)ÉĻŹö·½·ØÖʵƵÄH2æÉŅŌŗĶCOŌŚŅ»¶ØĢõ¼žĻĀŗĻ³É¼×“¼ŗĶ¶ž¼×ĆŃ£ØCH3OCH3£©¼°Šķ¶ąĢžĄąĪļÖŹ”£µ±Į½ÕßŅŌĪļÖŹµÄĮæ1:1“߻Ʒ“Ó¦£¬ĘäŌ×ÓĄūÓĆĀŹ“ļ100%£¬ŗĻ³ÉµÄĪļÖŹæÉÄÜŹĒ ”£
a.ĘūÓĶ b.¼×“¼ c.¼×Č© d.ŅŅĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ĆŗµÄĘų»ÆŹĒøߊ§”¢Ēå½ąµŲĄūÓĆĆŗĢæµÄÖŲŅŖĶ¾¾¶Ö®Ņ»”£
(1)ŌŚ250C 101kPaŹ±£¬H2ÓėO2»ÆŗĻÉś³É1mol H2O(g)·Å³ö241.8kJµÄČČĮ棬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ
___________
ÓÖÖŖ: ¢ŁC(s)£«O2(g)ØTCO2(g) ”÷H£½£393.5kJ/mol
¢ŚCO(g)£«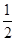 O2(g)ØTCO2(g) ”÷H£½£283.0kJ/mol
O2(g)ØTCO2(g) ”÷H£½£283.0kJ/mol
½¹ĢæÓėĖ®ÕōĘų·“Ó¦ŹĒ½«¹ĢĢåĆŗ±äĪŖĘųĢåČ¼ĮĻµÄ·½·Ø£¬C(s)£«H2O(g)ØTCO(g)£«H2(g) ”÷H=____kJ/mol
(2) COæÉŅŌÓėH2O(g)½ųŅ»²½·¢Éś·“Ó¦: CO(g)£«H2O(g) CO2(g)£«H2(g) ”÷H£¼0ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ£¬ĘšŹ¼Ź±n(H2O)=0.20mol£¬n(CO)£½0.10 mol,ŌŚ8000CŹ±“ļµ½Ę½ŗāדĢ¬£¬K£½1.0£¬ŌņĘ½ŗāŹ±£¬ČŻĘ÷ÖŠCOµÄ×Ŗ»ÆĀŹŹĒ_____________(¼ĘĖć½į¹ū±£ĮōŅ»Ī»Š”Źż)”£
CO2(g)£«H2(g) ”÷H£¼0ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ£¬ĘšŹ¼Ź±n(H2O)=0.20mol£¬n(CO)£½0.10 mol,ŌŚ8000CŹ±“ļµ½Ę½ŗāדĢ¬£¬K£½1.0£¬ŌņĘ½ŗāŹ±£¬ČŻĘ÷ÖŠCOµÄ×Ŗ»ÆĀŹŹĒ_____________(¼ĘĖć½į¹ū±£ĮōŅ»Ī»Š”Źż)”£
(3) ¹¤ŅµÉĻ“ÓĆŗĘų»ÆŗóµÄ»ģŗĻĪļÖŠ·ÖĄė³öH2£¬½ųŠŠ°±µÄŗĻ³É£¬ŅŃÖŖ·“Ó¦·“Ó¦N2(g)£«3H2(g 2NH3(g)£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ£¬øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚI”¢II”¢III½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ
2NH3(g)£Ø”÷H£¼0£©ŌŚµČČŻĢõ¼žĻĀ½ųŠŠ£¬øıäĘäĖū·“Ó¦Ģõ¼ž£¬ŌŚI”¢II”¢III½×¶ĪĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆµÄĒśĻßČēĻĀĶ¼ĖłŹ¾£ŗ
¢ŁN2µÄĘ½¾ł·“Ó¦ĖŁĀŹv1(N2)”¢vII(N2)”¢vIII(N2)“ӓ󵽊”ÅÅĮŠ“ĪŠņĪŖ________£»
¢ŚÓɵŚŅ»“ĪĘ½ŗāµ½µŚ¶ž“ĪĘ½ŗā£¬Ę½ŗāŅĘ¶ÆµÄ·½Ļņ ŹĒ________£¬²ÉČ”µÄ“ėŹ©ŹĒ________”£
¢Ū±Č½ĻµŚII½×¶Ī·“Ó¦ĪĀ¶Č(T2)ŗĶµŚIII½×¶Ī·“Ó¦ĖŁ¶Č£ØT3)µÄøßµĶ£ŗT2________T3Ģī”°”µ”¢=”¢<”±ÅŠ¶ĻµÄĄķÓÉŹĒ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŃŠ¾æĮņ¼°Ęä»ÆŗĻĪļµÄŠŌÖŹÓŠÖŲŅŖŅāŅ唣
£Ø1£©Cu2SŌŚøßĪĀĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗ
2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) ØSH=£773kJ/mol
µ±øĆ·“Ó¦ÓŠ1.2molµē×Ó×ŖŅĘŹ±,·“Ó¦ŹĶ·Å³öµÄČČĮæĪŖ kJ”£
£Ø2£©ĮņĖį¹¤ŅµÉś²śÖŠÉę¼°·“Ó¦£ŗ2SO2(g)+O2(g) 2SO3(g)£¬SO2µÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶Č”¢Ń¹ĒæµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£
2SO3(g)£¬SO2µÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶Č”¢Ń¹ĒæµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£
¢ŁŃ¹Ēæ£ŗP1 P2£ØĢī”°£¾”±”¢”°=”±»ņ”°<”±£©”£
¢ŚĘ½ŗā³£Źż£ŗAµć Bµć£ØĢī”°£¾”±”¢”°=”±»ņ”°<”±£©”£
¢Ū200”ęĻĀ£¬½«Ņ»¶ØĮæµÄSO2ŗĶO2³äČėĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬¾10minŗó²āµĆČŻĘ÷ÖŠø÷ĪļÖŹµÄĪļÖŹµÄĮæÅضČČēĻĀ±ķĖłŹ¾:
| ĘųĢå | SO2 | O2 | SO3 |
| ÅØ¶Č£Ømol/L£© | 0.4 | 1.2 | 1.6 |
 ”££ØŅŃÖŖøĆĪĀ¶ČĻĀH2SO3µÄµēĄė³£Źż£ŗKa1=1.0”Į10-2 mol/L£¬Ka2=6.0”Į10-3 mol/L£©
”££ØŅŃÖŖøĆĪĀ¶ČĻĀH2SO3µÄµēĄė³£Źż£ŗKa1=1.0”Į10-2 mol/L£¬Ka2=6.0”Į10-3 mol/L£©²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com