
| A. | 过滤时,漏斗的下端管口紧靠烧杯内壁 | |
| B. | 为了加快过滤速度,可用玻璃棒搅动过滤器中的液体 | |
| C. | 实验完毕后,用手直接取走蒸发皿 | |
| D. | 当蒸发皿中的固体完全蒸干后,再停止加热 |
分析 A.过滤液体时,要注意“一贴、二低、三靠”的原则;
B.为防止滤纸破损,不能用玻璃棒搅拌过滤器中的液体;
C.移动蒸发皿应该使用坩埚钳,不能使用手直接拿;
D.蒸发皿中出现多量固体时停止加热,用余热蒸干,防止温度过高,溶质分解.
解答 解:A.过滤液体时,要注意“一贴、二低、三靠”的原则,过滤时漏斗下端管口的尖嘴要紧靠承接滤液的烧杯内壁,可以使滤液顺着烧杯内壁流下,避免了滤液从烧杯中溅出,故A正确;
B.用玻璃棒搅拌过滤器中的液体可能将滤纸弄破,使实验失败,故B错误;
C.蒸发皿不能直接用手拿,应该使用坩埚钳,故C错误;
D.蒸发操作时,不能将蒸发皿中的液体蒸干,否则温度过高,溶质分解,所以当蒸发皿中有大量固体析出时停止加热,用余热蒸干,故D错误;
故选A.
点评 本题考查有关过滤和蒸发的操作,侧重于学生的分析能力和实验能力的考查,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键,题目难度不大.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源:2016-2017学年江苏省徐州市高一上第一次月考化学卷(解析版) 题型:选择题
下列化合物中属于共价化合物的是
A.NaCl B.NaOH C.CH4 D.(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
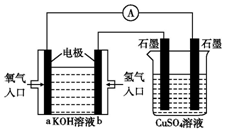 可用碱性氢氧燃料电池组装如图所示的装置:
可用碱性氢氧燃料电池组装如图所示的装置:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LCCl4含有的分子数为1 NA | |
| B. | 常温常压下,16g O2含有的原子数为1 NA | |
| C. | 通常状况下,1 NA 个CO2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5mol/L的BaCl2溶液中,含有Cl- 个数为1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,22.4LSO3含氧原子数为3NA | |
| B. | 将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA | |
| C. | 2 molSO2和1 molO2在密闭容器中加热(V2O5催化)充分反应后,容器内分子总数大于2NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ①② | C. | ④⑤ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水阴极产生氢气而得不到钠 | |
| B. | 铝制器皿不宜盛放酸性食物 | |
| C. | 铁制容器盛放和运输浓硫酸 | |
| D. | 镀锌铁桶镀层破损后铁仍不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A.在常温常压下,11.2 L N2含有分子数为0.5 NA
B.在常温常压下,22.4 L Ne含有分子数为NA
C.71 g Cl2所含原子数为2 NA
D.在同温同压下,相同体积的任何气体单质所含原子数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com