
���� ��1���ⲻ������ˮ���������л��ܼ���
��2��ʳ��������ˮ��
��3����ˮ��ˮ�ķе�ͣ�
��4��̼��Ƽ��ȷֽ�����CaO��
��5��CaCO3��������ˮ��Ca��OH��2����ˮ��
��� �⣺��1���ⲻ������ˮ���������л��ܼ�����Ӧѡ����ȡ���������ˮ�е⣬�ʴ�Ϊ����ȡ��
��2��ʳ��������ˮ����ѡ��������ȥʳ����Һ�е�ˮ���ʴ�Ϊ��������
��3����ˮ��ˮ�ķе�ͣ���ѡ����������ˮ���ʴ�Ϊ������
��4��̼��Ƽ��ȷֽ�����CaO����ѡ����ȷ���ȥ�������е�̼��ƣ��ʴ�Ϊ�����ȣ�
��5��CaCO3��������ˮ��Ca��OH��2����ˮ����ѡ����˷���ȥCa��OH��2��Һ��������CaCO3�����ʴ�Ϊ�����ˣ�
���� ���⿼����������ᴿ��Ϊ��Ƶ���㣬�������ʵ����ʡ����ʲ��졢�������뷽��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע����뷽����ԭ������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
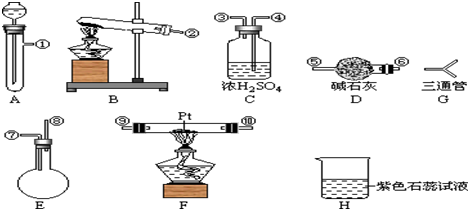
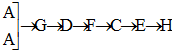 [��װ���Ⱥ�˳������]
[��װ���Ⱥ�˳������]�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ͬpH������HX��HY��ǰ�ߵ�Ka��С������ˮϡ�ͺ�pHֵ����ͬ����ǰ������ϡ�͵ı������� | |
| B�� | ��CH3COOH��CH3COONaŨ�Ⱦ�Ϊ0.1mol/L����ϵ�У��������ǿ��ʱ����Һ��PHֵ�����ϴ�仯 | |
| C�� | ��Na2HPO4ˮ��Һ�д��ڹ�ϵʽ��c��H3PO4��+c��H2PO4-��+c��HPO42-��+c��PO43-���Tc��Na+�� | |
| D�� | �����ܽ�ƽ��BaSO4�TBa2++SO42- �ij����ܽ�ƽ�ⳣ��Ϊ1.1��10-10��˵��������BaSO4��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ�Ⱦ�Ϊ0.1 mol•L-1��CH3COOH��CH3COONa��Һ�����������õ���Һ�У�c��CH3COOH��+c��CH3COO-���T0.2 mol•L-1 | |
| B�� | 0.1 mol•L-1 NaHCO3��Һ�У�c��Na+��=c��HCO3-��+c��H2CO3��+2c��CO32-�� | |
| C�� | 0.2 mol•L-1 HCl��Һ������0.1 mol•L-1 NaOH��Һ��Ϻ���Һ��pH=1 | |
| D�� | 0.1 mol•L-1��ˮ�е���0.1 mol•L-1��������Һ������ʱ��c��NH4+��=c��Cl-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ұ��ԭ������������������ԭ��Ӧԭ������һ�������½��������仯�����л�ԭ���� | |
| B�� | ��Щ���ý������������Ȼ�ԭ���Ļ�ԭ�� | |
| C�� | �õ������NaCl�ķ�����ұ�������� | |
| D�� | �ý�̿��һ����̼��ԭ�������ķ�����ұ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KCl��NaCl | B�� | KCl��NaCl��Na2SO4 | ||
| C�� | NaCl��Na2SO4��K2SO4 | D�� | KCl��Na2SO4��K2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
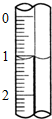 ��ʹ������к͵ζ����ⶨ���۰״�Ũ�ȣ�
��ʹ������к͵ζ����ⶨ���۰״�Ũ�ȣ����� ���ݣ�mL�� | 1 | 2 | 3 |
| V����Ʒ�� | 20.00 | 20.00 | 20.00 |
| V��NaOH�������ģ� | 14.95 | 16.05 | 15.95 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼ | B�� | ����ζ | ||
| C�� | ʪ��ĵ��۵⻯����ֽ | D�� | ����pH��ֽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
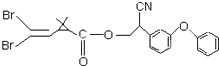 ����������һ���Ч���Ͷ���ɱ��������жԹ��ȶ�����������Ľṹ��ʽ��ͼ��ʾ�����жԸû�����������У���ȷ���ǣ�������
����������һ���Ч���Ͷ���ɱ��������жԹ��ȶ�����������Ľṹ��ʽ��ͼ��ʾ�����жԸû�����������У���ȷ���ǣ�������| A�� | ���ڷ����� | B�� | ÿһ�������ں�23��̼ԭ�� | ||
| C�� | ���ڸ߷��ӻ����� | D�� | ÿһ�������ں�7��̼̼˫�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com