
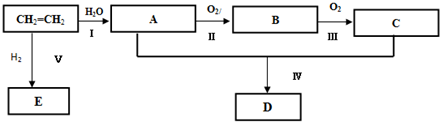
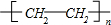 ;反应类型:加聚反应
;反应类型:加聚反应分析 乙烯含有碳碳双键,与水发生加成反应生成A为CH3CH2OH,乙醇发生催化氧化生成B为CH3CHO,乙醛进一步发生氧化反应生成C为CH3CHOOH,乙酸与乙醇发生酯化反应生成D为CH3COOCH2CH3,E为高分子化合物,乙烯发生加聚反应生成E为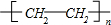 ,据此解答.
,据此解答.
解答 解:乙烯含有碳碳双键,与水发生加成反应生成A为CH3CH2OH,乙醇发生催化氧化生成B为CH3CHO,乙醛进一步发生氧化反应生成C为CH3CHOOH,乙酸与乙醇发生酯化反应生成D为CH3COOCH2CH3,E为高分子化合物,乙烯发生加聚反应生成E为 .
.
(1)A的结构简式为CH3CH2OH,含有官能团为:羟基,C为CH3COOOH,含有官能团为:羧基,
故答案为:CH3CH2OH;羟基;羧基;
(2)反应II是乙醇的催化氧化,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)反应IV是乙醇与乙酸发生酯化反应生成乙酸乙酯,反应方程式为:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,属于酯化反应,
故答案为:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化反应.
(4)反应V是乙烯发生加聚反应生成聚乙烯,反应化学方程式为:n H2C=CH2$\stackrel{一定条件}{→}$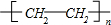 ,
,
故答案为:n H2C=CH2$\stackrel{一定条件}{→}$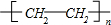 ,加聚反应;
,加聚反应;
(5)乙醇和钠反应的化学方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸性质与转化等,难度不大,有利于基础知识的巩固.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种气体质量相等 | B. | 三种气体的物质的量之比为16:2:1 | ||
| C. | 三种气体压强比为16:8:1 | D. | 三种气体体积比为1:8:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量是物质粒子的数量的简称 | |
| B. | 摩尔是用来描述物质所含微粒数目多少的基本物理量 | |
| C. | 我们把含有6.02×1023个粒子的任何粒子的集合体计量为1摩尔 | |
| D. | 1mol H2中含2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. 、
、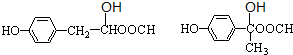 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +Br2→
+Br2→ ,反应类型为加成反应.
,反应类型为加成反应.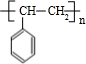 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2?Ca2++2OH- | B. | NaHCO3═Na++H++CO32- | ||
| C. | H2CO3?2H++CO32- | D. | Na2SO4═2Na++SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com