
| A. | 53 | B. | 78 | C. | 25 | D. | 184 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
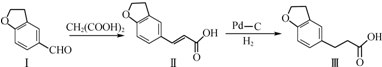
| A. | 与化合物Ⅰ互为同分异构体,且分子中含有2个醛基的芳香族化合物有9种 | |
| B. | 化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应 | |
| C. | 化合物Ⅱ中共含有4种官能团 | |
| D. | 可用溴水区分化合物Ⅱ和化合物Ⅲ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(×10-4 mol/L) | 10 | 4.05 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)(×10-3 mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| A. | 该反应转化较快,具有现实意义 | |
| B. | 催化转化器在冬季时对废气转化的效率比夏季更高 | |
| C. | 在该温度下,反应的平衡常数K=10000 | |
| D. | 2 s末的平均反应速率为v(NO)=3.75×10-4 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
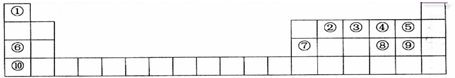
 ,其最高氧化物水化物与⑥号元素最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-_.
,其最高氧化物水化物与⑥号元素最高价氧化物水化物反应的离子方程式为Al(OH)3+OH-=[Al(OH)4]-_.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
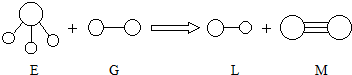
| A. | G是最活泼的非金属单质 | B. | L分子中有共价键 | ||
| C. | E能使紫色石蕊试液变蓝色 | D. | M化学性质很活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 服进肠胃的药剂根本不会直接进入人的膀胱中,Cu(OH)2悬浊液无法与葡萄糖作用 | |
| B. | 所用药剂具有毒性(含重金属元素Cu)和强腐蚀性(含NaOH),不能内服 | |
| C. | 该同学设计是正确的,但由于体温达不到令Cu(OH)2悬浊液与葡萄糖反应的温度,故检验不会成功 | |
| D. | 由于人们吃入的淀粉在体内也能水解成葡萄糖,会干扰检验的现象,检验应空腹进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电池工作时,MnO2失去电子 | |
| B. | 电池工作时,电子由锌经外电路流向MnO2 | |
| C. | 从反应方程式来看,不使用氢氧化钾,也不影响电流大小 | |
| D. | 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com