
【题目】下列离子方程式中书写正确的有几项![]()
![]() 固体与稀硝酸混合:
固体与稀硝酸混合:![]()
![]() 用过量氨水吸收烟道气中的
用过量氨水吸收烟道气中的![]() :
:![]()
![]() 将少量
将少量![]() 气体通入NaClO溶液中:
气体通入NaClO溶液中:![]()
![]() 已知
已知![]() ,向NaClO溶液中通入少量
,向NaClO溶液中通入少量![]() :
:![]()
![]() 铁屑溶于足量稀硝酸:
铁屑溶于足量稀硝酸:![]()
![]() 氯气溶于水:
氯气溶于水:![]()
![]() 实验室用
实验室用![]() 和
和![]() 制氨气:
制氨气:![]()
![]()
![]()
![]() 向
向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液至
溶液至![]() 恰好沉淀完全:
恰好沉淀完全:![]()
![]() 实验室制
实验室制![]() :
:![]() 浓
浓![]() 十
十![]()
![]()
![]()
![]() 溶液刻蚀铜制电路板:
溶液刻蚀铜制电路板:![]()
A.1项B.2项C.3项D.4项
【答案】A
【解析】
![]() 固体与稀硝酸混合,硫离子和亚铁离子都被硝酸氧化,故
固体与稀硝酸混合,硫离子和亚铁离子都被硝酸氧化,故![]() 错误;
错误;
![]() 用过量氨水吸收烟道气中的
用过量氨水吸收烟道气中的![]() ,反应生成亚硫酸铵,该反应的离子方程式为:
,反应生成亚硫酸铵,该反应的离子方程式为:![]() ,故
,故![]() 正确;
正确;
![]() 少量
少量![]() 气体通入NaClO溶液中,二氧化硫被氧化成硫酸根离子,故
气体通入NaClO溶液中,二氧化硫被氧化成硫酸根离子,故![]() 错误;
错误;
![]() 酸性
酸性![]() ,将少量
,将少量![]() 气体通入NaClO溶液,反应生成次氯酸和碳酸氢根离子,正确的离子方程式为:
气体通入NaClO溶液,反应生成次氯酸和碳酸氢根离子,正确的离子方程式为:![]() ,故
,故![]() 错误;
错误;
![]() 铁屑溶于足量稀硝酸,反应生成铁离子,故
铁屑溶于足量稀硝酸,反应生成铁离子,故![]() 错误;
错误;
![]() 氯气溶于水生成氯化氢和次氯酸,次氯酸不能拆开,故
氯气溶于水生成氯化氢和次氯酸,次氯酸不能拆开,故![]() 错误;
错误;
![]() 和
和![]() 制氨气的反应不是发生在水溶液中,无法书写离子方程式,故
制氨气的反应不是发生在水溶液中,无法书写离子方程式,故![]() 错误;
错误;
![]() 向
向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液至
溶液至![]() 恰好沉淀完全,
恰好沉淀完全,![]() 、
、![]() 的物质的量之比为1:2,反应生成氢氧化铝沉淀和一水合氨,正确的离子方程式为:
的物质的量之比为1:2,反应生成氢氧化铝沉淀和一水合氨,正确的离子方程式为:![]() ,故
,故![]() 错误;
错误;
![]() 实验室制
实验室制![]() ,HCl应该拆开,故
,HCl应该拆开,故![]() 错误;
错误;
![]() 溶液刻蚀铜制电路板,反应生成氯化亚铁和氯化铜,正确的离子方程式为:
溶液刻蚀铜制电路板,反应生成氯化亚铁和氯化铜,正确的离子方程式为:![]() ,故
,故![]() 错误;
错误;
根据分析可知,正确的有1个,
故选:A。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列电子式书写正确的是( )
①氧原子![]() ②过氧根离子
②过氧根离子![]() ③氢氧根离子
③氢氧根离子![]() ④钠离子
④钠离子![]() ⑤氢离子
⑤氢离子![]() ⑥铵根离子
⑥铵根离子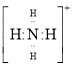 ⑦铝原子
⑦铝原子![]() ⑧溴离子
⑧溴离子![]()
A.①②③⑥⑦B.①③④⑥⑦⑧C.①③⑤⑥⑦⑧D.②③④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气中含有的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中的NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图所示。
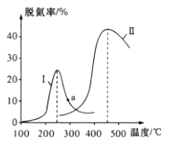
若温度低于200℃,图中曲线脱氯率随温度升高而变化不大的主要原因是___;判断a点对应的脱氮率是否为对应温度下的平衡脱氮率,并说明其理由:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应![]() 经2min后,B的浓度减少了0.6mol·L-1。下列说法正确的是( )
经2min后,B的浓度减少了0.6mol·L-1。下列说法正确的是( )
A.用A表示的化学反应速率是0.4mol·L-1·min-1
B.分别用B、C、D表示化学反应速率,其比是3:2:1
C.在2min末的反应速率用B表示是0.3mol·L-1·min-1
D.在这2min内B和C两物质的浓度都减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物、二氧化硫是造成大气污染的主要物质,某科研小组进行如下研究。
(1)已知:
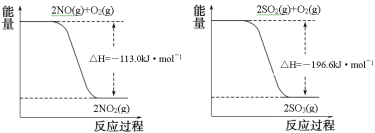
写出SO2(g)与NO2(g)反应生成SO3(g)和NO(g)的热化学方程式___。
(2)向容积为1L密闭容器中分别充入0.10molNO2和0.15molSO2,在不同温度下测定同一时刻NO2的转化率,结果如图所示。
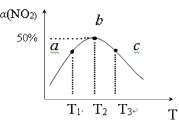
①a、c两点反应速率大小关系:υ(a)___υ(c)。(填“>”、“<”或“=”)
②温度为T2时从反应开始经过2min达到b点,用SO3表示这段时间的反应速率为___,此温度下该反应的平衡常数为___,若在此温度下,保持容器的容积不变,再向容器中充入0.20molNO2和0.30molSO2,NO2的转化率___。(填“增大”、“减小”或“不变”)
③NO2的转化率随温度升高先增大后减小的原因是:___。
(3)常温下用NaOH溶液吸收SO2,在吸收过程中,溶液pH随n(SO32-)∶n(HSO3-)变化关系如下表:
n(SO32-)∶n(HSO3-) | 91∶9 | 1∶1 | 9∶91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液呈中性时,溶液中离子浓度由大到小排列顺序为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家通过测量SiO2中26Al和10Be两种元素的比例来确定“北京人”年龄,这种测量方法叫铝铍测年法。关于26Al和10Be的说法不正确的是
A.10Be和9Be是中子数不同质子数相同的不同原子
B.10Be的原子核内中子数比质子数多
C.5.2 g26Al3+中所含的电子数约为1.2×1024
D.26Al和26Mg的质子数、中子数和核外电子数都不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种以液态肼(N2H4)为燃料,氧气为氧化剂,某固体氧化物为电解质的新型燃料电池。该固体氧化物电解质的工作温度高达700900℃时,O2可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。下列说法正确的是( )

A.电池内的O2由电极乙移向电极甲
B.电池总反应为N2H4+2O2=2NO+2H2O
C.当甲电极上有lmolN2H4消耗时,乙电极上有22.4LO2参与反应
D.电池外电路的电子由电极乙移向电极甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,将乙针筒内的物质压到甲针筒内,进行下表所列实验,对实验现象的描述错误的是
(气体在同温同压下测定)
![]()
选项 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
A | 20mLH2S | 10mLSO2 | 生成黄色固体,活塞自动向内压缩 |
B | 1g薄铜片 | 10mL12mol/L浓硝酸 | 生成棕色气体、溶液呈绿色,活塞自动外移,Cu有剩余 |
C | 30mLNO2 | 10mL水(液态) | 剩有无色气体,活塞自动向内压缩 |
D | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,最终沉淀转变为红褐色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在1L密闭容器中加amolSO2和bmolO2发生反应2SO2+O2![]() 2SO3,反应达到平衡时有cmolSO2发生了反应,试填下列空白:
2SO3,反应达到平衡时有cmolSO2发生了反应,试填下列空白:
(1)生成___molSO3;
(2)O2的转化率为___;
(3)平衡时容器内气体的总物质的量为___mol;
(4)达到平衡时,c(SO2)=___mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com