
分析 (1)a氯气泄露应通知关部门,迅速撤离事故现场;
b根据氯气能和碱、水反应,逆风减少氯气的吸入量;
c烧碱具有强烈的腐蚀性;
(2)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
(3)①根据氯化铵易分解和氯化氢与氨气易反应生成氯化铵分析;
②按照气体发生装置、除杂装置、性质检验装置、尾气处理装置等顺序组装仪器;
③根据方程式结合M=$\frac{m}{M}$进行计算
解答 解:(1)a氯气泄露应通知关部门,迅速撤离事故现场,故a选;
b氯气能和碱、水反应,逆风减少氯气的吸入量,故b选;
c烧碱具有强烈的腐蚀性,能够腐蚀皮肤,故c不选;
故选:ab;
(2)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
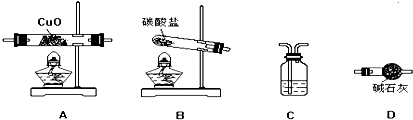
(3)①制备氨气时应用碳酸铵和氢氧化钙反应,而不能用氯化铵,因氯化铵分解生成的氨气和氯化氢气体易反应而重新生成氯化铵,反应的方程式为HCl+NH3=NH4Cl,
故答案为:否;HCl+NH3=NH4Cl;
②氨气还原氧化铜时,应先制备氨气,并用碱石灰干燥氨气,生成的氨气在加热条件下与氧化铜反应,生成的水用碱石灰吸收以测定生成水的质量,最后用浓硫酸吸收氨气并防止空气中的水和CO2进入D装置以免造成误差,
故答案为:BDADC;浓硫酸;防止空气中的水和CO2进入D装置,吸收多余的氨气;
③根据反应的方程式计算
2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$N2+3Cu+3H2O
3mol 3mol
$\frac{m(CuO)}{M(Cu)+16}$ $\frac{m({H}_{2}O)}{18}$
M(CuO)=$\frac{18m(CuO)}{m({H}_{2}O)}$-16;
故答案为:$\frac{18m(CuO)}{m({H}_{2}O)}$-16;
点评 本题考查了氨气的制备和性质的检验,熟悉制备原理是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 若5.6LN2中含有n个氮分子,则阿伏加德罗常数一定为4n | |
| B. | 4.6gNa与100 mL含0.1mol HCl的盐酸溶液反应,转移电子数目为0.2NA | |
| C. | 14g乙烯和丙烯的混合气体中所含分子总数为0.5NA | |
| D. | 标准状况下,22.4LCCl4含有的分子总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在周期表中过渡元素可作为催化剂 | |
| B. | 化学键可以使离子结合,也可以使原子结合 | |
| C. | 常温常压下,相同体积的O2和O3具有相同的分子数 | |
| D. | F2、Cl2、Br2、I2共价键逐渐增强,熔点依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n=m+1 | B. | n=m+10 | C. | n=m+11 | D. | n=m+25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,2.24LC6H14中含有1.9NA个共用电子对 | |
| B. | 7.8gNa2O2固体中含阴离子数目为0.1NA | |
| C. | 含36.5gHCl的浓盐酸与足量的二氧化锰作用,能产生0.25NA个氯气分子 | |
| D. | 5.6gFe与足量的氯气反应转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使 pH 试纸呈红色的溶液:Fe2+、NH4+、Cl-、NO3- | |
| B. | pH=13的溶液:S2-、SO32-、SO42-、Na+ | |
| C. | 使红色石蕊试纸变蓝色的溶液:K+、HCO3-、Br-、Ba2+ | |
| D. | 含有溶质为K2SO4的溶液:AlO2-、Na+、Al3+、Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.右图是元素周期表的一部分. 查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 零 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molC2H6O中含有C-C键的数目一定为NA | |
| B. | 25℃,pH=12的NaHCO3溶液中含有OH-的数目为0.01NA | |
| C. | 标准状况下,2.24L异丁烷含有的分子数目为0.1NA | |
| D. | 常温常压下,0.3molNO2与足量H2O充分反应,转移电子的数目为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com