
| A. | CH4与C2H4 | |
| B. | CH3-CH=CH-CH3 与 CH3-CH2-CH2-CH3 | |
| C. | O2与O3 | |
| D. | C2H6与C3H8 |
分析 结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;互为同系物的物质满足以下特点:结构相似、化学性质相似、分子式通式相同、分子式不同、物理性质不同,研究对象是有机物.
解答 解:A.CH4通式为CnH2n+2,C2H4通式为CnH2n,二者通式不同,不是同系物,故A错误;
B.CH3-CH=CH-CH3含有碳碳双键,通式为CnH2n,CH3-CH2-CH2-CH3没有碳碳双键,通式为CnH2n+2,二者通式不同,不是同系物,故B错误;
C.O2与O3都是氧元素的不同单质,二者互为同素异形体,故C错误;
D.分子式为C2H6与C3H8的烃都符合CnH2n+2,一定为链状烷烃,碳原子数不同,一定互为同系物,故D正确.
故选D.
点评 本题考查了同系物的判断,题目难度不大,注意掌握同系物的概念及判断方法,明确结构相似的含义:如果含有官能团,含有官能团的种类及数目一定相同.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应中旧键断裂需要吸收能量,新键形成需放出能量,所以总能量不变 | |
| B. | 上述热化学方程式中的△H的值与反应物的用量无关 | |
| C. | 该反应为放热反应 | |
| D. | 反应物的总能量高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同二氧化碳一样,二氧化硅分子是由一个硅原子和两个氧原子构成的 | |
| B. | 通常状况下,二氧化碳为气态,二氧化硅为固体 | |
| C. | SiO2同CO2一样也能与CaO反应生成盐 | |
| D. | SiO2仅用来表示二氧化硅的组成,其基本结构单元为正四面体,不仅存在于二氧化硅晶体中,而且存在于所有硅酸盐矿石中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
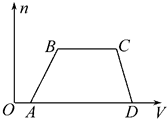
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | (1)有机物A的相对分子质量为:90. |
| (2)将此9.0gA在足量纯O2充分燃烧,并使 其产物依次通过足量无水硫酸铜粉末、足量石灰水,发现硫酸铜粉末增重5.4g,石灰水中有30.0g白色沉淀生成. | (2)9.0g有机物A完全燃烧时,经计算: 生成CO2共为0.3mol, 生成的H2O0.3mol. 有机物A的分子式C3H6O3. |
| (3)经红外光谱测定,证实其中含有O-H键,-COOH基团,C-H键;经核磁共振氢谱的测定,其核磁共振氢谱图 如:  | (3)A的结构简式 . . |
| (4)如果经红外光谱测定,A的一种同分异构体中,存在O-H键, 还含有醛基,C-O键,  核磁共振氢谱的测定, 其核磁共振氢谱图如右: | (4)A的这种同分异构体的结构简式为: CH2(OH)CH(OH)CHO. |
| (5)如果经红外光谱测定,A的一种同分异构体中,存在O-H键,还含有C=O,C-O键, 核磁共振氢谱的测定, 其核磁共振氢谱图如:  | (5)A的这种同分异构体的结构简式为: . . |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H5CH2CH2OH与C6H5OH互为同系物 | |
| B. | CH3CHO与CH3COOH在一定条件下均能与新制氢氧化铜反应 | |
| C. |  与 与  互为同分异构体 互为同分异构体 | |
| D. | H2O与D2O互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

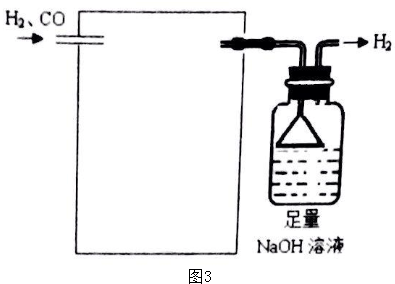
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com