
��16�֣�ijǿ������ҺX����Ba2+��Al3+��NH4+��Fe2����Fe3+��CO32-��SO32-��SO42-��Cl-��NO3-�е�һ�ֻ��֣�ȡ����Һ��������ʵ�飬ʵ���������£�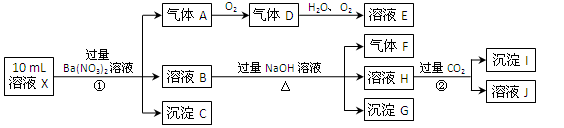
����������Ϣ���ش��������⣺
(1)���������У���ҺX�г�H����϶����е������� ������ȷ���Ƿ��е�����(Q)�� ����Ҫȷ����Q(����ֹһ�֣�����ѡһ��)�����ڣ���ɿ��Ļ�ѧ������ ��
(2)����G�Ļ�ѧʽΪ ��
(3)д���й����ӷ���ʽ����������A ��
�� ��
(4)����ⶨA��F��I��Ϊ0.01mol��10mL X��Һ��n(H��)��0.04mol��������C���ʵ���(�����������������ij��ֵ) ������Q����һ���� ��(����ֹһ�ֿ��ܣ����һ���������)
��16�֣���1��Al3+��NH4+��Fe2+��SO42-�� Fe3+ ��Cl����
ȡ����X��Һ�����Թ��У����뼸��KSCN����Һ�����ɫ˵����Fe3+������ȡ����B��Һ�����Թ��У����뼸��AgNO3��Һ���ް�ɫ����˵����Cl��(ֻҪ���һ�ּ��ɵ÷֣�������ǿ��ȡX��Һ��B��Һ��ûȡ��ȡ�����÷�) (����������Ҳ��)
��2��Fe(OH)3
��3��3Fe2��+NO3��+4H����3Fe3++NO��+2H2O�� AlO2��+CO2+2H2O��Al(OH)3��+HCO3��
��4����0.07mol��Fe3+���ߣ�0.07mol��Cl��(ֻҪд��һ�ּ��ɵ÷�)
����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
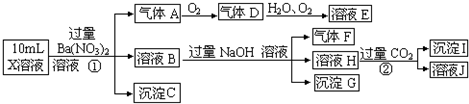
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| H | + 4 |
| O | 2- 3 |
| O | 2- 3 |
| O | 2- 4 |
| O | - 2 |
| O | - 3 |


�鿴�𰸺ͽ���>>
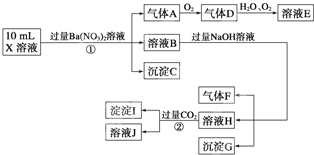
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
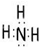
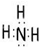
�鿴�𰸺ͽ���>>
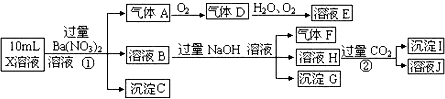
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
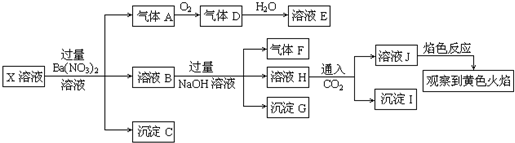
| A��X�п϶�����Na+��Fe2+��Al3+��NH4+��SO42- | B������F����������ֱ����������D | C������Cһ����BaSO4������Gһ����Fe��OH��3������Iһ����Al��OH ��3 | D��X�в���ȷ���������� Al3+��Na+��K+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���㽭ʡ�����и�����ѧ��������У������ѧ�Ծ��������棩 ���ͣ�ѡ����
ijǿ������ҺX�п��ܺ���Fe2+��A13+��NH4+��CO32�D��SO32�D��SO42�D��C1�D�е������֣���ȡX��Һ��������ʵ�飬ʵ����̼��������£�

����˵����ȷ����
A������A��NO2 B��X�п϶�����Fe2+��A13+��NH4+��SO42�D
C����ҺE������F���ܷ�����ѧ��Ӧ D��X�в���ȷ���������� A13+��C1�D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com