
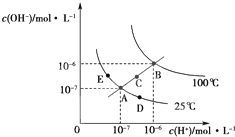
| A、图中五点KW间的关系:B=C=A=D=E |
| B、若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合,溶液显酸性 |
| C、若从A点到C点,可采用:温度不变在水中加入适量的NH4Cl固体 |
| D、若从A点到D点,可采用:温度不变在水中加入少量的酸 |


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:高中化学 来源: 题型:
| A、将表面有铜绿[Cu2(OH)2CO3]的铜器放入硝酸中浸泡,除去铜绿 |
| B、大量使用煤发电是形成雾霾的主要原因,天然气、煤气大量泄露遇到明火会爆炸 |
| C、利用化学反应可实现12C到14C的转化,高炉炼铁是炼铁最常用的方法 |
| D、青铜(铜锡合金)是一种复合材料,二氧化硅可以做光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 60 | 240 | 930 | 1000 |
| 残留固体质量(g) | 19.7 | 16.1 | 8.1 | 8.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水滴入石蕊试液中,只能看到试液变红 |
| B、铜丝在Cl2中燃烧后向集气瓶中加水,溶液呈蓝绿色,说明CuCl2是蓝绿色的 |
| C、饱和氯水光照时有气泡产生,该气体为氯气 |
| D、钠在氯气中燃烧,火焰呈黄色,集气瓶中生成白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用N2浓度的减少表示的平均反应速率为0.2mol?L-1?s-1 |
| B、2s时N2的转化率为40% |
| C、2s时混合气体中n(N2):n(H2):n(NH3)═3:9:4 |
| D、2s时NH3的浓度为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
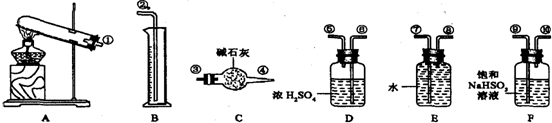
 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
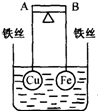 如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )
如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)( )| A、杠杆为导体和绝缘体时,均为A端高B端低 |
| B、杠杆为导体和绝缘体时,均为A端低B端高 |
| C、当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低 |
| D、当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com