
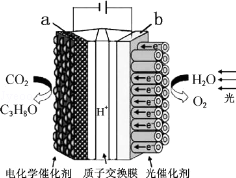
 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )| A. | 该装置将化学能转化为光能和电能 | |
| B. | 该装置工作时,H+从a极区向b极区迁移 | |
| C. | 每生成3mol O2,有88gCO2被还原 | |
| D. | a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O |
分析 A.电解池是将电能转化为化学能的装置;
B.电解池工作时,电解质溶液中阳离子向阴极移动;
C.根据转移电子相等计算被还原二氧化碳质量;
D.a电极是阴极,阴极上二氧化碳得电子和氢离子反应生成C3H8O和水.
解答 解:A.电解池是将电能转化为化学能的装置,该装置有外接电源,所以是电解池,是将化学能转化为电能的装置,故A错误;
B.电解池工作时,电解质溶液中阳离子向阴极移动,所以该装置工作时,H+从b极区向a极区迁移,故B错误;
C.根据转移电子相等得被还原m(CO2)=$\frac{3mol×4}{6}×44g/mol$=88g,故C正确;
D.a电极是阴极,阴极上二氧化碳得电子和氢离子反应生成C3H8O和水,电极反应式为3CO2+18H++18e-=C3H8O+5H2O,故D错误;
故选C.
点评 本题考查电解原理,为高频考点,侧重考查基本概念、基本计算,难点是电极反应式的书写,易错点是离子移动方向判断,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镀锌层破损后即对镀锌铁(白铁)制品失去保护作用 | |
| B. | 制备氢氧化铁胶体时,应向FeCl3溶液中滴加NaOH溶液,并继续煮沸至液体呈红褐色 | |
| C. | 用托盘天平称取5.85g NaCl,称量时砝码放在右盘,氯化钠放在左盘 | |
| D. | 用灼烧闻气味的方法可以区别棉花和羊毛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
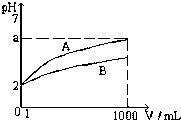 T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示
T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O | |
| B. | 稀盐酸除铁锈:6H++Fe2O3=2Fe3++3H2O | |
| C. | 金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.7g金属铝变成铝离子时失去的电子数目为0.2NA | |
| B. | 16g CH4与18 g NH4+ 所含质子数相等 | |
| C. | 标准状况下,22.4 L汽油所含的分子数为NA | |
| D. | 在0℃,1.01×105Pa时,11.2L氮气所含的原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol O3的质量为16 g | B. | 32 g O2中含有的氧分子数为2NA | ||
| C. | 1 g H2中含有电子数为1NA | D. | 3.01×1023个铜原子的质量为64 g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com