
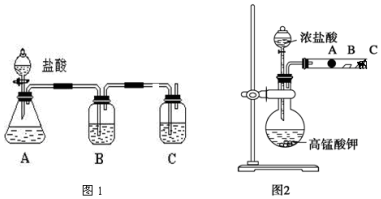
分析 (1)根据信息知道:甲同学根据元素非金属性与对应最高价含氧酸之间的关系如图1装置来一次性完成C、Si三种非金属元素的非金属性强弱比较,根据强酸制弱酸来回答即可;B的作用是除去二氧化碳中氯化氢,C中二氧化碳和硅酸钠反应;
(2)根据氧化性强的单质可以将氧化性弱的单质从其盐中置换出来结合反应产物来分析.
解答 解:(1)根据题干信息:甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究,碳酸酸性强于硅酸,最高价氧化物对应水化物酸性越强,则原子的非金属性越强,依据强酸制弱酸来设计反应;A装置用来制取二氧化碳,故A为碳酸钙,盐酸易挥发,故B的作用是除去二氧化碳中氯化氢,故B为饱和碳酸钠溶液,C为硅酸钠溶液,二氧化碳和硅酸钠发生反应离子方程式为:SiO32-+CO2+H2O═H2SiO3↓+CO32-;
故答案为:最高价氧化物对应水化合物酸性H2CO3>H2SiO3;CaCO3;饱和NaHCO3溶液;Na2SiO3溶液;除去CO2气体中混有的HCl气体;SiO32-+CO2+H2O═H2SiO3↓+CO32-;
(2)根据题干信息:乙同学设计了如图2装置来验证卤族元素性质的递变规律,所以乙同学的实验原理是非金属性强的元素对应的单质可置换出非金属性弱的元素对应的单质,高锰酸钾和浓盐酸反应会产生氯气,氯气具有氧化性,能将溴离子,碘离子氧化为对应的单质,即A处:Cl2+2Br-=2Cl-+Br2,棉花变成橙黄色,B:Cl2+2I-=2Cl-+I2,试纸变蓝色,氯气污染环境,不能直接排放,故C处蘸有碱液的棉花吸收尾气;
故答案为:非金属性强的元素对应的单质可置换出非金属性弱的元素对应的单质;棉花变成橙黄色;Cl2+2I-=2Cl-+I2;吸收尾气.
点评 本题将元素及其化合物、元素周期律与非金属性强弱比较的实验设计结合起来,具有较强的综合性,有一定的难度,注意实验设计的原理和方法.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 10L0.10mol/LCH3COOH 溶液 | B. | 2L 0.05mol/L H2SO4溶液 | ||
| C. | lL0.10mol/LHNO3溶液 | D. | 2L0.1mol/LHCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 建筑中使用的铝合金门窗比钢门窗更耐腐蚀 | |
| B. | 窗帘上直接受阳光照射的一面布料容易褪色 | |
| C. | 肉放在冷冻箱中要比放在保鲜箱中存放的时间更长久 | |
| D. | 实验室用硫酸溶液与锌粒反应制取氢气,反应一段时间后,气泡变得稀少了(锌粒还有剩余),如果添加一些适当浓度的硫酸溶液到反应容器中,气泡又重新增多起来 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱金属原子最外电子层上都只有1个电子,容易失去 | |
| B. | 碱金属在常温下易被氧化 | |
| C. | 碱金属单质的密度小,熔点和沸点低 | |
| D. | 碱金属原子的核电荷数比较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com