
分析 Cl元素全部被氧化,则Cl失去电子,Cl元素的化合价升高,Cl元素全部被还原,则Cl得到电子,Cl元素的化合价降低,以此来解答.
解答 解:A.Cl2+H2O=HCl+HClO,该反应中Cl元素化合价由0价变为-1价、+1价,所以Cl元素部分被氧化部分被还原;
B.2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应中部分Cl元素的化合价从-1价升高到0价,部分不变价,则Cl部分被氧化;
C.2KClO3 $\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,该反应中Cl元素化合价由+5价变为-1价,所以氯元素得电子化合价降低,全部被还原;
D.2H2SO4+2KCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnSO4+K2SO4+Cl2↑+2H2O,该反应中Cl元素化合价由-1价变为0价,所以Cl元素失电子化合价升高,全部被氧化;
故答案为:D; C; A B; A.
点评 本题考查氧化还原反应,侧重考查基本概念,明确概念内涵是解本题关键,知道常见元素化合价.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
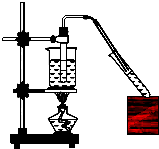 实验室用如图所示的装置制取乙酸乙酯.
实验室用如图所示的装置制取乙酸乙酯.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2+Ba(OH)2═BaCl2+Mg(OH)2↓ | B. | CO2+2NaOH═Na2CO3+H2O | ||
| C. | CaCO3 $\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | H2+CuO $\frac{\underline{\;\;△\;\;}}{\;}$H2O+Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
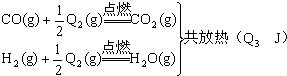
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液使紫色石蕊试液变蓝;结论:溶液一定呈碱性 | |
| B. | 无色溶液焰色反应呈紫色(透过蓝色钴玻璃观察),结论:溶液中一定含有K+ | |
| C. | 在无色溶液中加入Na2CO3溶液产生白色沉淀;结论:溶液中一定含有Ca2+ | |
| D. | 在无色盐溶液中加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝;结论:溶液一定含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
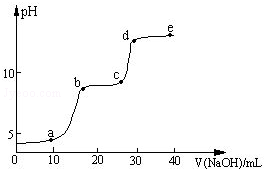
| 较大量存在的含金属元素的离子 | 检验方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 78gNa2O2固体中阴离子的个数为2NA | |
| B. | 标准状况1.12L氯气与H2O反应,反应中转移的电子数为0.1NA | |
| C. | CO2通过Na2O2使其增重ag时,反应中转移的电子数为$\frac{a{N}_{A}}{56}$ | |
| D. | 60gSiO2含有的化学键数目为4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com