
【题目】构成金属键的基本微粒是( )
A.分子B.原子C.阳离子和阴离子D.金属阳离子和自由电子
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1mol/L的是( )
A. 含Na+为2mol的Na2SO4溶液
B. 将80g SO3溶于水并配成1L的溶液
C. 将0.5mol/L的某饱和溶液100mL,加热蒸发掉50g水后的溶液
D. 将58.5gNaCl溶于1L水所得的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学需要借助化学专用术语来描述,下列有关化学用语的使用正确的是( )
A. NH4Cl的电子式:![]() B. S2–的结构示意图:
B. S2–的结构示意图: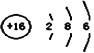
C. CO2的结构式:O=C=OD. 中子数为20的氯原子:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)检验火柴头中氯元素的其中一种方法是将火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含氯元素。写出上述检验原理的总离子方程式:___________________________。
(二)肼(N2H4)作为一种重要的氮氢化合物,氢质量分数高达12.5%,完全分解产物为H2和N2,是一种理想的液体氢源。N2H4分解过程中发生完全分解和不完全分解。
完全分解: N2H4(g) ![]() N2(g) + 2H2(g) ΔH1 = -50.6 kJ·mol-1 I
N2(g) + 2H2(g) ΔH1 = -50.6 kJ·mol-1 I
不完全分解: 3N2H4(g) ![]() 4NH3(g) + N2(g) ΔH2 II
4NH3(g) + N2(g) ΔH2 II
反应II的焓变不易测量,现查表得如下数据:
2NH3(g) ![]() N2(g) + 3H2(g) ΔH3 = +92 kJ·mol-1 (该反应实际未发生)
N2(g) + 3H2(g) ΔH3 = +92 kJ·mol-1 (该反应实际未发生)
(1)反应II在__________(填高温、低温或任意温度)条件下可以自发进行。
(2)在体积固定的密闭容器中,以Ir/Al2O3为催化剂,在不同温度下(催化剂均未失活)分解等量N2H4(一开始体系中无其他气体),测得反应相同时间后的N2H4、NH3和H2体积分数如图1所示:

①下列说法正确的是_____________
A.据图可知200℃时,反应 I的活化能低于反应II的活化能
B.300℃后N2H4的体积分数略有提高,可能由于反应II逆向移动导致
C.换用选择更高的Ni/Ir复合催化剂可提高N2H4的平衡转化率
D.400℃是该制氢工艺比较合适的生产温度
②若某温度下在1 L体积固定的密闭容器中加入1molN2H4,反应一段时间后达到平衡状态,此时H2与NH3的物质的量均为0.4mol。请计算该温度下反应 I的平衡常数KC=___________________(Kc为用气体的浓度表示的平衡常数)
③若在600~1000°C下进行上述实验,请预测并在上图中补充H2体积分数的变化趋势_______。
(3)近期,来自四位非洲的女孩打造了一台靠尿液驱动的发电机,其原理是把尿液以电解的方式分离出提供设备发电使用的氢气的技术,同时将尿液脱氮(转化为大气循环的无污染气体)减轻生活污水处理。以纯尿液为电解液(以NH4+表示尿液中氮元素的存在形式),写出该电解过程的总反应方程式:________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ某溶液中只可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+、Cl-、OH-、CO32-。当加入一种淡黄色固体并加热时,有刺激性气体放出和白色沉淀产生,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如下图所示。该淡黄色物质做焰色反应实验显黄色。可知溶液中含有的离子是________________;所含离子的物质的量浓度之比为____________;所加的淡黄色固体是______________。

Ⅱ.实验室采用滴定法测定某水样中亚硫酸盐含量:

(1)滴定时,KIO3和KI作用析出I2,完成并配平下列离子方程式:__IO3-+____I-+____===____I2+____H2O。
(2)反应(1)所得I2的作用是_________________________。
(3)滴定终点时,100mL的水样共消耗x mL标准溶液。若消耗1mL标准溶液相当于SO32-的质量1g,则该水样中SO32-的含量为________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 石灰乳与过量碳酸氢钙溶液反应:HCO3—+Ca2++OH-==CaCO3↓+H2O
B. 向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O(沸水)![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
C. 二氧化碳通入足量的氢氧化钠溶液:CO2 + OH-═ HCO3-
D. 氧化钠与盐酸反应:O2-+2H+ ==== H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)用“>”或“<”填写下表。
第一电离能 | 熔点 | 沸点(同压) | 键能 |
P____S | MgO____CaS | CF4____SiCl4 | H-Cl____ H-Br |
(2)一种制取NH2OH的反应为2NO2-+4SO2 + 6H2O+ 6NH3 = 4SO![]() +6NH4++2NH2OH。
+6NH4++2NH2OH。
①N、H、O的电负性从小到大的顺序为____。
②NH3分子的空间构型为____。
③NH2OH极易溶于H2O,除因为它们都是极性分子外,还因为____。
(3)配合物K[PtCl3(NH3)]中[PtCl3(NH3)]-的结构可用示意图表示为____(不考虑空间构型)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答:
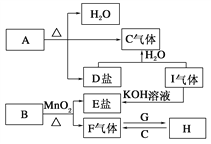
(1)画出G离子结构示意图________;
(2)写出B、I的化学式B________,I________;
(3)写出H的一种用途__________________________________;
(4)写出A受热分解的化学方程式_________________________;
(5)若10g的C6H12O6在氧气中充分燃烧,将产物全部与足量的H充分反应,反应后固体增重____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝。关于![]() Lv 的叙述错误的是
Lv 的叙述错误的是
A. 原子序数 116B. 中子数 177
C. 核外电子数 116D. 核电荷数 293
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com