
【题目】某实验小组同学进行如下实验,以检验化学反应中的能量变化。
(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是______热反应, Ba(OH)28H2O与NH4Cl反应时,需要将固体研细其目的是________________.反应过程______ (填“①”或“②”)的能量变化可用图表示。

(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的是_________(填序号)。

(3)将CH4设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中____(填A或B)处电极入口通甲烷,其电极反应式为_____________________ 。当消耗标况下甲烷33.6L时,假设能量转化率为90%,则导线中转移电子的物质的量为_________mol。

(4)如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:

①当电极c为Al、电极d为Cu、电解质溶液为稀硫酸时,写出该原电池正极的电极反应式为_______________。
②当电极c为Al、电极d为Mg、电解质溶液为氢氧化钠溶液时,该原电池的正极为_______;该原电池的负极反应式为_____________________________。
【答案】放 扩大接触面积,提高反应速率 ① ② A CH4﹣8e—+10OH﹣=CO32—+7H2O 10.8 2H++2e—═H2↑ Mg Al+4OH—﹣3e—=AlO2—+2H2O
【解析】
根据反应物和生成物具有总能量的大小判断吸热反应还是放热反应;根据原电池原理分析电池的正负极及书写电极反应式;根据电极反应式计算电子的转移。
(1)温度升高,说明反应为放热;将固体研细其目的是扩大接触面积,提高反应速率;图示中反应物的总能量高于生成物的总能量,反应为放热反应,反应①为放热反应,故答案为: 放;扩大接触面积,提高反应速率;①;
(2)为了验证Fe3+与Cu2+氧化性强弱,可以利用原电池原理,装置②中发生的总反应为Cu与Fe3+反应生成Fe2+,根据氧化还原反应原理知强化剂的氧化性强于氧化产物的氧化性,所以验证了Fe3+与Cu2+氧化性强弱,故答案为②;
(3)由图所示,电子从A极流出,则A电极入口通甲烷,其电极反应式为:CH4﹣8e—+10OH﹣=CO32—+7H2O;根据电极反应知:n(8e-)=8n(CH4)=![]() ,若能量转化率为90%,则导线中转移电子的物质的量为12mol×90%=10.8mol;
,若能量转化率为90%,则导线中转移电子的物质的量为12mol×90%=10.8mol;
(4)①正极氢离子得电子,电极反应式为 2H++2e—═H2↑;
②因为Al和氢氧化钠溶液反应、而Mg不反应,所以负极是铝、Mg作正极;该原电池的负极反应式为: Al+4OH—﹣3e—=AlO2—+2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图是采用新能源储能器件将CO2转化为固体产物,实现CO2的固定和储能灵活应用的装置。储能器件使用Li-CO2电池,组成为:钌电极/CO2饱和的LiClO4-DMSO电解液/锂片。下列说法不正确的是
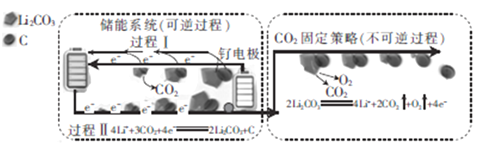
A. Li-CO2电池的电解液由LiClO4和DMSO溶于水得到
B. CO2的固定中,每转移8 mol e-,生成6 mol气体
C. 过程Ⅱ中化学能转化为电能
D. 过程Ⅰ的钌电极的电极反应式为2Li2CO3+C-4e-═4Li++3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示。下列说法一定正确的是( )
A. 最高正化合价:Z>X
B. X、Y、Z的单质中,Z的熔点最高
C. 若X为非金属元素,则离子半径:Xn->Ym->Zm-
D. 若X为金属元素,则X、Y、Z的最高价氧化物对应水化物中,Y的碱性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小。下列能源中属于未来新能源的是 ( )
①天然气 ②煤 ③潮汐能 ④核能 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④B.⑤⑥⑦⑧C.③⑤⑥⑦⑧D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是
Na2S+2CO2↑。下列有关说法正确的是
A. 1mol/LNa2SO4溶液中含氧原子的数目一定大于4NA
B. 1L0.1mol/LNa2S溶液中含阴离子的数目小于0.1NA
C. 生成1mol氧化产物时转移电子数为4NA
D. 通常状况下11.2LCO2中含质子的数目为11NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化石燃料是有机物的重要来源,从煤和石油获取的有机物苯和乙烯等简单有机物还是合成其他有机物的原料。如图的转化关系中,已知C能使碳酸钠溶液释放出CO2,反应①②反应机理类似且原子利用率均为100%,请回答下列问题:

(1)有机物A中含有的官能团名称是_________________。
(2)反应④的反应类型为_________________。
(3)请设计一种能验证B与C混合物中是否含物质B的实验方法_________________。
(4)下列说法正确的是_________________。
A.乙烯与氧气在催化剂作用下反应也可以生成C
B.纯C在16.6℃ 以下呈冰状固体
C.在制备D时,D中常混有一些挥发出来的反应物,可以通过加入NaOH溶液振荡再分液的方法提纯
D.石油裂解气通过净化和分离也能得到丙烯这样的短链烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 200mL 含等物质的量 HBr 和H2SO3 的溶液中通入 0.01molCl2,有一半 Br-变为 Br2(已知 Br2 能氧化 H2SO3),原溶液中 HBr 和 H2SO3 的浓度都等于 :
A. 0.0075molL-1B. 0.0018mol L-1C. 0.04mol L-1D. 0.08molL L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在无色透明的强酸性溶液里大量共存的是
A.MnO4-、K+、Na+、SO42-B.Na+、K+、HCO3-、Cl-
C.Mg2+、NH4+、NO3-、Cl-D.Cu2+、K+、OH-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com