
| A、32 | B、16 | C、8 | D、4 |
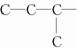 ,
, ,则A有四种结构,B有四种结构,醇和酸若重新组合,可形成的酯共有16种.
,则A有四种结构,B有四种结构,醇和酸若重新组合,可形成的酯共有16种.

 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它可与1mol O2完全反应(点燃) |
| B、它是4mol H |
| C、它是与16g CH4所含的H的数目相同 |
| D、它与2NA个H2SO4所含的H的数目相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干燥的Cl2和氯水均能使鲜花褪色 |
| B、向碘水中通入SO2,碘水褪色说明SO2具有漂白性 |
| C、向FeBr2溶液中滴加少量氯水,溶液变浅黄色是因为生成了Br2 |
| D、将Cl2通入AgNO3溶液中不会有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 光照 |
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.001 0 | 0.001 6 | 0.002 0 | 0.002 0 |
| A、前20 min内的反应速率v(H2O)=5.0×10-5 mol?L-1?min-1 |
| B、达到平衡时,至少需要从外界吸收能量0.968 kJ |
| C、增大c(H2O),可以提高水的分解率 |
| D、催化效果与Cu2O颗粒的大小有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
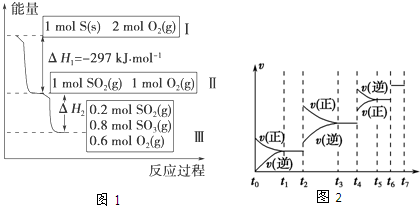
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com