
【题目】(加试题 )M结构简式如图所示,是牙科粘合剂,X是高分子金属离子螯合剂,以下是两种物质的合成路线:


已知:I.A为烯烃,C属于环氧类物质,G分子中只有1种氢原子
II.
III.
IV.R1CHO+R2NH2![]() R1CH=NH2+H2O
R1CH=NH2+H2O
(1)A→B的反应类型是_________,C→D的可采用的反应条件是____________。
(2)下列说法正确的是______。
A.B中含有的官能团是碳碳双键和氯原子
B.J可与Na2CO3溶液反应,1 mol J与饱和溴水反应最多消耗4mol Br2
C.在一定条件下,F可以发生缩聚反应
D.X可发生加成、氧化和消去反应
(3)Q+Y→X的化学方程式是_________________________________________。
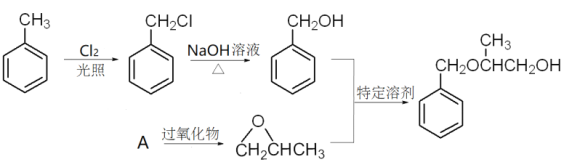
(4)请设计以甲苯和A作为原料制备 的合成路线流程图(无机试剂任用)____________________________。
的合成路线流程图(无机试剂任用)____________________________。
(5)写出符合下列条件的K的同分异构体:____________________________
①能发生银镜反应,不能发生水解反应;
②含有五元碳环,核磁共振氢谱有5组峰;
③结构中无-C=C-OH和-O-O-
【答案】取代反应 NaOH/H2O,△ A、B 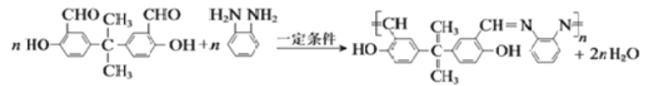

【解析】
A的分子式为C3H6的烯烃,所以A的结构简式为:CH3CH=CH2,A与氯气发生取代反应生成B,B为ClCH2CH=CH2,ClCH2CH=CH2与过氧化物反应生成C,C为![]() ,
,![]() 在氢氧化钠的溶液中发生水解反应生成
在氢氧化钠的溶液中发生水解反应生成![]() ,G分子中只有1个氢原子,分子式为C3H6O,所以G为
,G分子中只有1个氢原子,分子式为C3H6O,所以G为![]() ,
,![]() 与HCN发生加成反应,反应后酸化得到E,E为
与HCN发生加成反应,反应后酸化得到E,E为![]() ,
,![]() 在浓硫酸的催化作用下发生消去反应生成F,F为
在浓硫酸的催化作用下发生消去反应生成F,F为![]() ,
,
![]() 与苯酚反应生成J和水,J为
与苯酚反应生成J和水,J为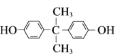 ,根据已知II,
,根据已知II, 与三氯甲烷在氯化铝作用下反应生成N,分子式为C17H16O2Cl4,根据后面X的结构简式可知,取代位置在酚羟基的邻位,故N为
与三氯甲烷在氯化铝作用下反应生成N,分子式为C17H16O2Cl4,根据后面X的结构简式可知,取代位置在酚羟基的邻位,故N为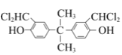 ,
, 在氢氧化钠水溶液中发生水解反应酸化得到Q为
在氢氧化钠水溶液中发生水解反应酸化得到Q为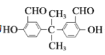 ,
, 在一定条件下与Y发生缩聚反应生成
在一定条件下与Y发生缩聚反应生成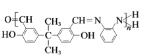 ,
,![]() 与
与![]() 发生酯化反应生成K,K与
发生酯化反应生成K,K与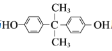 反应生成M,据此答题。
反应生成M,据此答题。
(1)由分析可知,A→B的反应为CH3CH=CH2与氯气发生取代反应生成ClCH2CH=CH2,C→D发生的是卤代烃的水解反应,所以反应的条件为NaOH/H2O,△,故答案为:取代反应;NaOH/H2O,△。
(2)A.B为ClCH2CH=CH2,含有的官能团是碳碳双键和氯原子,故A正确;
B.J为 ,含有酚羟基,可与Na2CO3溶液反应,1molJ与饱和溴水反应最多消耗4molBr2,故B正确;
,含有酚羟基,可与Na2CO3溶液反应,1molJ与饱和溴水反应最多消耗4molBr2,故B正确;
C.F为![]() ,含有碳碳双键和羧基,在一定条件下可以发生加聚反应,故C错误;
,含有碳碳双键和羧基,在一定条件下可以发生加聚反应,故C错误;
D.根据X的结构简式,含有碳氮双键,可以发生加成反应;含有酚羟基,可以发生氧化反应,但不能发生消去反应,故D错误。
故答案为:AB。
(3)
Q+Y→X的化学方程式是
 ,故答案为:
,故答案为: 。
。
(4)根据题中已知信息,甲苯和A作为原料制备 的合成路线流程图为
的合成路线流程图为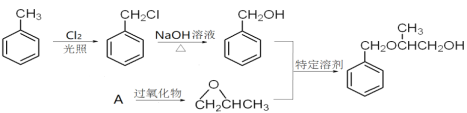 ,故答案为:
,故答案为: 。
。
(5)K的分子式为C7H10O3,①能发生银镜反应,不能发生水解反应;说明含有醛基,不含有酯基;②含有五元碳环,核磁共振氢谱有5组峰;说明有5种不同环境的氢原子;③结构中无-C=C-OH和-O-O-;符合条件的同分异构体为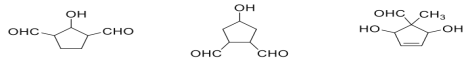 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. Na 与 H2O 的反应是熵增的放热反应,该反应能自发进行
B. 饱和 NaCl 溶液加入浓盐酸析出晶体,易溶电解质也存在溶解平衡
C. FeCl3 和 MnO2 均可加快 H2O2 分解,同等条件下二者对 H2O2 分解速率的改变相同
D. Mg(OH)2 固体在溶液中存在平衡:Mg(OH)2(s)Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:A(S)+B(g)![]() C(g)+ D(g)ΔH<0,达到平衡时,改变单一条件,下列说法正确的是()
C(g)+ D(g)ΔH<0,达到平衡时,改变单一条件,下列说法正确的是()
A. 恒温环境下加压,体系的平均相对分子质量一定升高
B. 反应速率再次满足υC:υD=1:1时,则反应达到平衡状态
C. 恒温恒容下,当物质A的质量不再改变,则反应达到平衡状态
D. 物质A由块状变为粉末状,正反应速率加快,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用如下装置所示方法制备氯气:
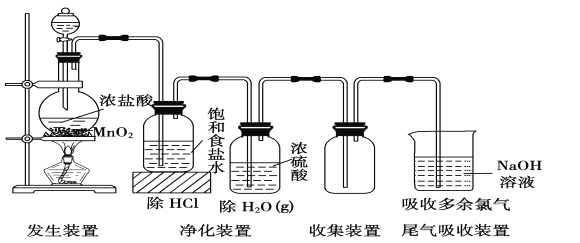
(1)1molMnO2和4mol浓盐酸制得的氯气的产量往往远低于1mol,原因可能是_________________;
(2)若改用NaCl固体、浓硫酸和MnO2一起加热,理论上氯元素利用率可以达到100%,试用化学反应方程式表示原因____________________________________;
(3)若在分液漏斗下方接一段毛细管插入圆底烧瓶底部,不需加热也可获得均匀稳定干燥的氯化氢气流,则分液漏斗和圆底烧瓶中应该盛放的试剂分别是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,具有容量高、循环稳定性好、成本适中等重要优点。镍钴锰三元材料中Ni为主要活泼元素,通常可以表示为:LiNiaCobMncO2,其中a+b+c=1,可简写为LiAO2。充电时总反应为LiAO2 + nC = Li1-xAO2 + LixCn(0<x<1),工作原理如下图所示,则以下说法正确的是( )

A. 放电时Ni元素最先失去电子
B. 放电时电子从a电极由导线移向b电极
C. 充电时的阳极反应式为LiAO2 - xe-= Li1-xAO2 + xLi+
D. 充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】凯夫拉是一种高强度、耐腐蚀的芳纶纤维,军事上称为“装甲卫士”,但长期浸渍在强酸或强碱中强度有所下降。下表中是凯夫拉的两种结构:
| 芳纶1313(PMTA) | 芳纶1414(PPTA) |
结构 简式 |
|
|
以下说法不正确的是
A. PMTA和PPTA互为同分异构体
B. “芳纶1313”、“芳纶1414”中的数字表示苯环上取代基的位置
C. 凯夫拉在强酸或强碱中强度下降,可能与“![]() ”的水解有关
”的水解有关
D. 以![]() 和
和![]() 为原料制备PPTA的反应为缩聚反应
为原料制备PPTA的反应为缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】软锰矿在生产中有广泛的应用。

(1)过程Ⅰ:软锰矿的酸浸处理
① 酸浸过程中的主要反应(将方程式补充完整):2FeS2+___MnO2+__===____Mn2++2Fe3++4S+___。
② 生成的硫附着在矿粉颗粒表面使上述反应受阻,此时加入H2O2,利用其迅速分解产生的大量气体破除附着的硫。导致H2O2迅速分解的因素是______。
③矿粉颗粒表面附着的硫被破除后,H2O2可以继续与MnO2反应,从而提高锰元素的浸出率,该反应的离子方程式是______。
(2)过程Ⅱ:电解法制备金属锰,金属锰在______(填“阳”或“阴”)极析出。
(3)过程Ⅲ:制备Mn3O4

下图表示通入O2时pH随时间的变化。15~150分钟滤饼中一定参与反应的成分是______,判断的理由是______。

(4)过程Ⅳ:制备MnCO3
MnCO3难溶于水、能溶于强酸,可用MnSO4溶液和NH4HCO3溶液混合制备。每制得1 mol MnCO3,至少消耗a mol/L NH4HCO3溶液的体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇被称之为继紫杉醇之后又一绿色抗癌药物,目前在保健品、食品、化妆品等诸多领域都有了广泛的应用。其合成路线如下:

回答下列问题:
(1)物质A中官能团的电子式为____,合成路线中设置反应①的目的是____。
(2)化合物X的蒸气密度是相同条件下H2密度的51倍,则X的结构简式为____。
(3)在反应①~④中属于取代反应的有____。
(4)Y核磁共振氢谱有____组峰,其峰面积之比为____。任写一种与Y核磁共振氢谱峰组数相同、峰面积之比也相同的同分异构体的结构简式____。
(5)反应⑤的化学方程式为____。
(6)白藜芦醇与溴水反应时,1 mol白藜芦醇最多可消耗____mol Br2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用![]() 表示阿佛加德罗常数,下列说法正确的是( )
表示阿佛加德罗常数,下列说法正确的是( )
A.常温常压下,11.2 L氧气含有的原子数为![]() 个
个
B.标准状况下,0.2 mol ![]() 的体积为4.48 L
的体积为4.48 L
C.2.3 g金属钠变为离子失去电子数为![]() 个
个
D.常温常压下,![]() 个氢分子的质量为2 g
个氢分子的质量为2 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com