
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 电离能 I1 I2 I3 I4 … |
| In/kJ.mol-1 578 1817 2745 11578 … |
 ,下列叙述正确的有
,下列叙述正确的有 的熔点(填>、=或<),其原因是
的熔点(填>、=或<),其原因是查看答案和解析>>
科目:高中化学 来源: 题型:
| 各组中物质的编号 | ||||
| 晶体类型 | 分子晶体 | 原子晶体 | 离子晶体 | 金属晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
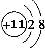
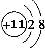
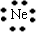
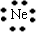
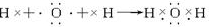
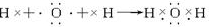


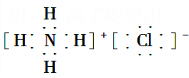
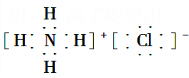
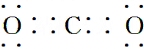
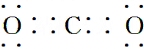
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化锰 | B、氯酸钾 | C、红磷 | D、硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有些物质是由原子直接构成,如金刚石、水晶等;有些物质是由分子直接构成,如干冰、氯化铵等;有些物质是由离子直接构成的,如食盐、烧碱等 | B、BF3、H2O、SiCl4、PCl5四种分子中所有原子都满足最外层为8电子结构 | C、非金属氧化物不都是酸性氧化物;碱性氧化物都是金属氧化物 | D、硫单质的熔点比钠单质的熔点高,这是由于前者比后者有更大的范德华力所致 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com