
【题目】(普通)化合物H是重要的有机物,可由E和F在一定条件下合成:(部分反应物或产物省略,另请注意箭头的指向方向)
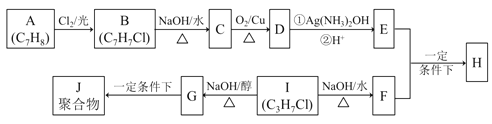
已知以下信息:
i.A属于芳香烃,H属于酯类化合物。
ii.I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)E的含氧官能团名称 ,B的结构简式 。
(2)B → C和G → J两步的反应类型 , 。
(3)① E + F → H的化学方程式 。
② I → G 的化学方程式 。
(4)I的同系物K比I相对分子质量大28,K有多种同分异构体。
①K的同分异构体共 种。
②若K不能发生消去反应,则K的结构简式为_________ _。
【答案】
(1)羧基;![]()
(2)取代反应;加聚反应或聚合反应;
(3)![]() +CH3CH(OH)CH3
+CH3CH(OH)CH3![]()
![]() +H2O;
+H2O;![]()
(4)① 8;②(CH3)3CCH2Cl
【解析】
试题分析:A属于芳香烃,分子式为C7H8,则A为![]() ,B与氯气在光照条件下发生甲基上取代反应生成B,结合B的分子式可知B为
,B与氯气在光照条件下发生甲基上取代反应生成B,结合B的分子式可知B为![]() ,B发生水解反应生成C为
,B发生水解反应生成C为![]() ,C发生催化氧化生成D为
,C发生催化氧化生成D为![]() ,D与银氨溶液反应、酸化得到E为
,D与银氨溶液反应、酸化得到E为![]() .I的分子式为C3H7Cl,核磁共振氢谱为二组峰,且峰的面积比为6:1,则I为CH3CHClCH3,I发生水解反应得到F为CH3CH(OH)CH3,E与F发生酯化反应生成H为
.I的分子式为C3H7Cl,核磁共振氢谱为二组峰,且峰的面积比为6:1,则I为CH3CHClCH3,I发生水解反应得到F为CH3CH(OH)CH3,E与F发生酯化反应生成H为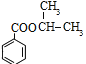 。I发生消去反应生成G为CH2=CHCH3,G发生加聚反应生成J为
。I发生消去反应生成G为CH2=CHCH3,G发生加聚反应生成J为![]() 。
。
(1)通过以上分析知,E为![]() ,含有官能团为羧基,B结构简式为
,含有官能团为羧基,B结构简式为![]() 。
。
故答案为:羧基;![]() ;
;
(2)B→C和G→J两步的反应类型分别为取代反应、加聚反应。
故答案为:取代反应;加聚反应;
(3)①E+F→H的化学方程式为:![]() ,
,
②I→G 的化学方程式:![]() 。
。
故答案为:![]() ;
;![]() ;
;
(4)I(CH3CHClCH3)的同系物K比I相对分子质量大28,则K的分子式为C5H11Cl,
①可以看作C5H12被取代产物,正戊烷被取代有3种,异戊烷被取代有4种,新戊烷被取代有1种,故K的同分异构体有8种。
故答案为:8;
②若K不能发生消去反应,则K的结构简式为(CH3)3CCH2Cl。
故答案为:(CH3)3CCH2Cl。


科目:高中化学 来源: 题型:
【题目】某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):

(1) 哪一时间段(指①0~1、②1~2、③2~3、④3~4、⑤4~5 min,下同)反应速率最大 ,(填序号,下同) ,原因是 。
(2) 哪一段时段的反应速率最小 ,原因是 。
(3) 求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变,不要求写出计算过程) 。
(4) 如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液:[A.蒸馏水 B.NaCl溶液 C Na2CO3溶液 D.CuSO4溶液
你认为可行的是(填编号) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
(1) NaClO2的化学名称为_______。
(2)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________。增加压强,NO的转化率______(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______ (填“增大”“不变”或“减小”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pe如图所示。

①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________(填“增大”、“不变”或“减小”)。
②反应ClO2+2SO32===2SO42+Cl的平衡常数K表达式为___________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______。
②已知下列反应:
SO2(g)+2OH (aq) ===SO32 (aq)+H2O(l) ΔH1
ClO (aq)+SO32 (aq) ===SO42 (aq)+Cl (aq) ΔH2
CaSO4(s) ===Ca2+(aq)+SO42(aq)ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO (aq) +2OH (aq) === CaSO4(s) +H2O(l) +Cl (aq)的ΔH=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、有机物分子中的一个碳原子所连的4个原子或原子团均不相同时,该碳原子称为手性碳原子,含有手性碳原子的化合物具有光学活性,某有机物X(结构如下)具有光学活性(式中标有*号的碳为手性碳原子),欲使其保持光学活性,发生以下 (选填序号)反应,该有机物仍一定具有光学活性。
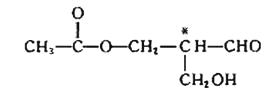
A.消去反应 | B.水解反应 | C.银镜反应 | D.酯化反应 |
Ⅱ、写出由1-溴丁烷和必要的无机试剂制取1,2-二溴丁烷的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H = —49.0kJ/mo1.测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H = —49.0kJ/mo1.测得CO2和CH3OH(g)的浓度随时间变化如图所示。
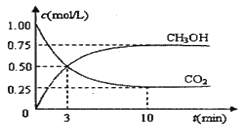
(1)从反应开始到平衡,氢气的平均反应速率v(H2)= mol/(L·min)
(2)该反应的平衡常数为 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入lmol CO2和3mol H2
(4)已知在常温常压下:
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g) △H= —1275.6kJ/mol
②H2O(g)=H2O(1) △H= —44.0kJ/mol
则甲醇的燃烧热化学方程式为: ;
(5)如果燃烧甲醇会造成大量化学能损失,如果以甲醇和空气为原料,以氢氧化钠为电解质溶液设计成原电池将有很多优点,请书写出该电池的负极反应:___________________
(6)常温下,某水溶液M中存在的离子有:Na+、A—、H+、OH—。若该溶液M由 pH=3的HA溶液![]() mL与pH=11的NaOH溶液
mL与pH=11的NaOH溶液![]() mL混合反应而得,则下列说法中正确的是 __。
mL混合反应而得,则下列说法中正确的是 __。
A.若溶液M呈中性,则溶液M中c(H+)+c(OH—)=2×10—7mol·L-1
B.若V1=V2,则溶液M的pH一定等于7
C.若溶液M呈酸性,则V1一定大于V2
D.若溶液M呈碱性,则V1一定小于V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ已知NiXO晶体晶胞结构为NaCl型(如图),由于晶体缺陷,x值小于1。测知NiXO晶体x=0.88,晶胞边长为4.28×10-10m 求:(已知:![]() =1.4)
=1.4)
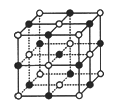
(1)晶胞中两个Ni原子之间的最短距离___________m(精确至0.01)。
(2)与O2-距离最近且等距离的Ni离子围成的几何体形状___ ____。
(3)晶体中的Ni分别为Ni2﹢、Ni3﹢,求此晶体的化学式_________。
(4)已知,NiO晶体熔点大于NaCl,主要原因是______________________________。
Ⅱ金晶体是面心立方最密堆积,立方体的每个面上5个金原子紧密堆砌(如图,其余各面省略),金原子半径为A cm,求:
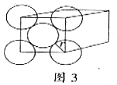
(1)金的密度为___________![]() 。(用带A计算式表示)
。(用带A计算式表示)
(2)金原子空间占有率为___________。(用带A计算式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4,较多的CuSO4和少量Na2SO4。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀H2SO4、NaOH溶液等试剂)
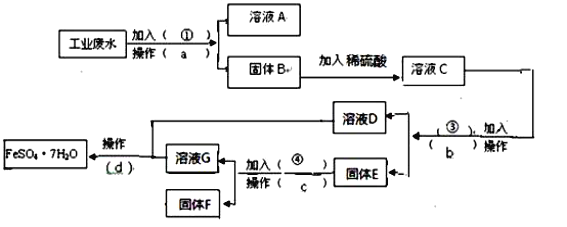
(1)操作a的名称为 ,所需要的玻璃仪器除烧杯外还需要 。
(2)固体E的成分为 ,加入的试剂④为 ,发生的化学方程式为 。
(3)加入试剂①的目的是 。
(4)从溶液D和溶液G中得到FeSO4.7H2O晶体的操作为 、 、 、洗涤、干燥。
(5)若废水中硫酸亚铁、硫酸铜和硫酸钠组成的混合溶液,其中c(Cu2+)=0.1 mol/L,c(Fe2+)=0.4 mol/L,
c(SO42-)= 0.6 mol/L,已知氢离子浓度忽略不计,则c(Na+)为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com