
分析 (1)根据抗酸药物有效成分能中和胃里过多的盐酸分析;碳酸镁和盐酸反应生成氯化镁和水、二氧化碳,氢氧化铝和盐酸反应生成氯化铝和水;
(2)根据淀粉在人体内在酶的作用水解最终转化成葡萄糖判断;
(3)嚼碎后能增大固体表面积;
解答 解:(1)碳酸镁、氢氧化铝都能中和胃里过多的盐酸;碳酸镁与盐酸反应生成氯化镁、二氧化碳气体和水,碳酸镁需要保留化学式,反应的离子方程式为MgCO3+2HCl=MgCl2+H2O+CO2↑,氢氧化铝和盐酸反应生成氯化铝和水,反应的离子方程式为:Al(OH)3+3HCl═AlCl3+3H2O,故答案为:MgCO3+2H+=Mg2++H2O+CO2↑;Al(OH)3+3H+═Al3++3H2O;
(2)淀粉在人体内在酶的作用水解最终转化成葡萄糖,其分子式为:C6H12O6,故答案为:C6H12;
(3)嚼碎后能增大固体表面积,从而能加快与胃酸的反应速率.答:嚼碎后能增大固体表面积,加快反应速率.
点评 本题较为综合,主要考查酸碱盐之间的复分解反应及化学方程式的书写等知识,注意利用化学知识来解决生活中的问题,注意化学方程式的书写重要知识点,题目难度不大.


科目:高中化学 来源: 题型:推断题
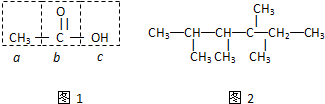
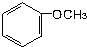 .
.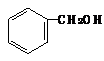 .
.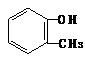 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液中:Na+、Fe2+、SO42-、Cl- | |
| B. | 使紫色石蕊试纸变红的溶液中:K+、Fe2+、NO3-、Ca2+ | |
| C. | 常温下PH=12的溶液中:Na+、I-、NO3-、Cl- | |
| D. | 与Al反应放出H2的溶液中:Na+、SO42-、ClO-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入溴水通入澄清石灰水 | |
| B. | 点燃罩上涂有澄清石灰水的烧杯 | |
| C. | 点燃罩上干冷烧杯罩上涂有澄清石灰水的烧杯 | |
| D. | 点燃罩上涂有澄清石灰水的烧杯 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
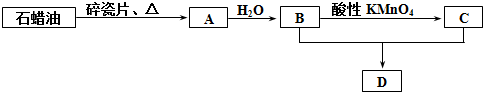
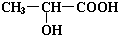 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键属于化学键,但比较弱 | |
| B. | 任何物质中都一定含有化学键 | |
| C. | NaOH中有离子键和共价键,则NaOH既属于离子化合物,又属于共价化合物 | |
| D. | Na2O2中既有离子键,又有非极性共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com