
| A.反应C(s)+CO2(g)=2CO(g);△H>0,在任何条件下均不能自发进行 |
| B.铅蓄电池在放电过程中,溶液的PH值增加 |
| C.常温下,在0.1mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 |
| D.温度一定时,水的离子积常数Kw不随外加酸(碱)浓度的改变而改变 |
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源:不详 题型:填空题

 Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;
Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
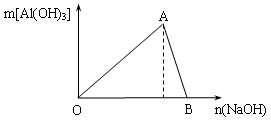
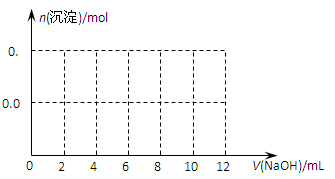
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.实验①中,反应生成的Mn2+可能是该反应的催化剂 |
| B.实验②中,该反应是太阳能转变为光能 |
| C.实验③中,有气泡产生的棒是铁棒 |
| D.实验④中,加入的水是反应的催化剂,且该反应能自发进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
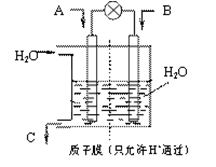
 N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,若 c (NO2) =" 0.0300" mol·L-1,
N2O4(g) △H <0的平衡常数 K=13.3,则该条件下密闭容器中N2O4和NO2的混合气体达到平衡时,若 c (NO2) =" 0.0300" mol·L-1,查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 的原料。已知:
的原料。已知: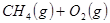
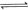



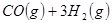




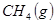 与
与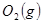 反应生成
反应生成 的热化学方程式为 。
的热化学方程式为 。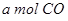 与
与 ,在不同压强下合成甲醇。
,在不同压强下合成甲醇。 的平衡转化率与温度、压强的关系如下图所示:
的平衡转化率与温度、压强的关系如下图所示: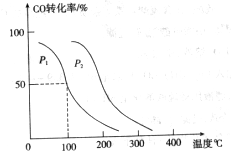

 (填“<”、“>”或“=”)
(填“<”、“>”或“=”) 、
、 压强时,平衡常数为 (用含
压强时,平衡常数为 (用含 的代数式表示)。
的代数式表示)。 电极通入的
电极通入的 为 ,电极反应式是 。
为 ,电极反应式是 。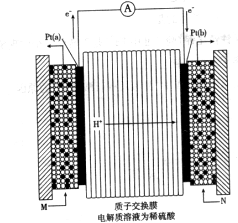
 溶液,当得到
溶液,当得到 铜时,参加反应的气体
铜时,参加反应的气体 的体积应为
的体积应为  (标准状况)。
(标准状况)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
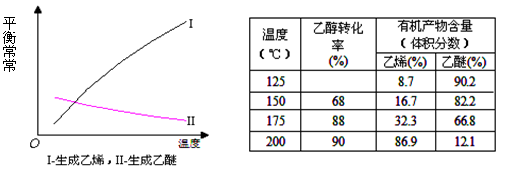
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.二氧化碳能溶于水,可用于生产碳酸型饮料 |
| B.固体二氧化碳俗称干冰,可用于人工降雨 |
| C.二氧化碳用于灭火是因为降低了可燃物的着火点 |
| D.超临界二氧化碳作萃取溶剂用于从天然产物提取和净化活性组分 |
 CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,测得C02和CH3OH(g)的浓度随时间变化如图所示。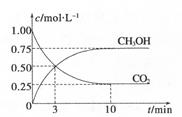
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com