
| A. | 使用SO2漂白过的物品在使用过程中会慢慢恢复为漂白前的颜色 | |
| B. | 向含有纯碱的废水中加入适量生石灰,可以消除水中的污染 | |
| C. | 大量焚烧田间秸秆会促进雾霾的形成 | |
| D. | 用热碱水吸收有利于除去手上的油脂形成的污渍 |
分析 A.二氧化硫具有漂白性,且为暂时性漂白,是二氧化硫和有机色素结合生成不稳定的化合物,受热分解重新恢复原来的颜色;
B.生石灰和水反应生成氢氧化钙,氢氧化钙和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠;
C.根据大量焚烧田间秸秆会产生大量烟尘判断;
D.纯碱溶液中碳酸根离子水解显碱性,水解过程是吸热过程,加热促进水解,油脂在碱中水解生成溶于水的物质;
解答 解:A.二氧化硫具有漂白性,且为暂时性漂白,二氧化硫能使有色物质褪色,加热颜色恢复,所以使用SO2漂白过的物品在使用过程中会慢慢恢复为漂白前的颜色,故A正确;
B.生石灰和水反应生成氢氧化钙,氢氧化钙和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,CaO+H2O=Ca(OH)2,CaCO3+Ca(OH)2=CaCO3↓+2NaOH,生成的氢氧化钠是强碱具有强腐蚀性,不能消除水的污染,故B错误;
C.大量焚烧田间秸秆会产生大量烟尘导致可吸入颗粒物增加而产生雾霾而影响空气质量,故C正确;
D.纯碱溶液中碳酸根离子水解显碱性,CO32-+H2O?HCO3-+OH-,水解过程是吸热过程,加热促进水解碱性增强,油脂在碱中水解生成溶于水的物质,便于洗去,故D正确;
故选B.
点评 本题主要考查了化学与生活、生产实践之间的联系,注意二氧化硫的漂白原理,碳酸钠水解显碱性,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.010mol/(L.s) | B. | v(O2)=0.010mol/(L.s) | ||
| C. | v(NO)=0.0010mol/(L.s) | D. | v(H2O)=0.045mol/(L.s) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
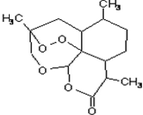 青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )| A. | 分子式是C15H22O5 | |
| B. | 易溶于水,乙醇和乙醚 | |
| C. | 含有-O-O-键,具有较强的氧化性 | |
| D. | 1mol青蒿素可以和1molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两溶液中水的电离程度相同 | B. | 水的离子积常数为1.0×10-(a+b) | ||
| C. | CH3COOH的电离常数为$\frac{(1{0}^{-2a})}{c}$ | D. | 两溶液中c(CH3COO-)=c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
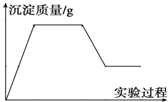 有一包白色固体物质,可能含有CuSO4、K2SO4、Na2CO3、Ca (NO3)2、KCl 中的一种或几种.将该白色固体少量溶于水中,得到无色透明溶液,取100mL该溶液先滴加足量硝酸钡溶液,再滴加足量稀硝酸,实验过程中沉淀质量的变化如图所示:
有一包白色固体物质,可能含有CuSO4、K2SO4、Na2CO3、Ca (NO3)2、KCl 中的一种或几种.将该白色固体少量溶于水中,得到无色透明溶液,取100mL该溶液先滴加足量硝酸钡溶液,再滴加足量稀硝酸,实验过程中沉淀质量的变化如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别Na2CO3和NaHCO3可用Ba(OH)2或Ca(OH)2溶液 | |
| B. | 除去Na2CO3固体中混有的少量NaHCO3,可采用加热法 | |
| C. | CO2中混有少量HCl、SO2等气体时,可用饱和NaHCO3溶液提纯气体 | |
| D. | 将澄清石灰水滴入NaHCO3溶液中,开始时发生反应的离子方程式为:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠溶液跟过量的饱和石灰水反应 HCO3-+Ca2++OH-═CaCO3↓+2H2O | |
| B. | 向NaHSO4溶液中滴加Ba(OH)2溶液显中性H++SO42-+-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 氯化亚铁溶液中通入氯气 Fe2++Cl2═Fe3++2Cl- | |
| D. | 苛性钾溶液中加入稀盐酸 H++OH-═H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com