
【题目】amolFeS与bmolFe3O4投入到VL cmol/L的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为
A.![]()
B.(a+3b)mol
C.![]()
D.(cV-3a-9b)mol
【答案】A
【解析】
反应中硝酸起氧化、酸性作用,未被还原的硝酸将转化为Fe(NO3)3中,由Fe元素守恒计算未被还原的硝酸的物质的量;起氧化剂作用的硝酸生成NO,根据电子转移守恒,可以用a、b表示计算NO的物质的量,根据氮元素守恒可知,未被还原的硝酸物质的量=原硝酸总物质的量-NO的物质的量
根据元素守恒可知,n[Fe(NO3)3]=n(Fe)=amol+3bmol=(a+3b)mol,所以未被还原的硝酸的物质的量=3(a+3b)mol;起氧化剂作用的硝酸生成NO,根据电子转移守恒可知,铁和硫元素失电子数等于硝酸得电子数,铁元素失电子的物质的量为![]() ;NO的物质的量为
;NO的物质的量为![]() ,未被还原的硝酸的物质的量为
,未被还原的硝酸的物质的量为![]() 。
。
答案选A。


科目:高中化学 来源: 题型:
【题目】化学学习小组进行如下实验。
【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变 化)。限选试剂和仪器:0.20mol/LH2C2O4 溶液、0.010mol/L KMnO4 溶液(酸性)、蒸馏水、 试管、量筒、秒表、恒温水浴槽
(1)上述实验①②是探究 对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则 a 为 ;乙是实验需要测量的物理量,则表 格中“乙”应填写 。
【测定 H2C2O4·xH2O 中 x 值】 已知:M(H2C2O4)=90g/mol
称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液。
②取 25.00 mL 待测液放入锥形瓶中,再加入适的稀 H2SO4
③用浓度为 0.05000 mol·L-1 的 KMnO 标准溶液进行滴定;
(2)请写出与滴定有关反应的离子方程式
(3)某学生的滴定方式(夹持部分略去)如下,最合理的是 (选填 a、b)。


(4)由右图可知消耗 KMnO4 溶液体积为 mL;
(5)滴定过程中眼睛应注视_________________;
(6)通过上述数据,求得 x= 。以标准 KMnO4 溶液滴定样品溶液的浓度,未用 标准 KMnO4 溶液润洗滴定管,引起实验结果 (偏大、偏小或没有影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以纯碱溶液为原料,通过电解的方法可制备小苏打,原理装置图如下:

上述装置工作时,下列有关说法正确的是
A. Na+由乙池穿过交换膜进入甲池
B. 甲池电极反应:4CO32-+2H2O-4e-=4HCO3-+O2↑
C. 乙池电极接电池正极,气体X为H2
D. NaOH溶液Y比NaOH溶液Z浓度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产符合人类需要的特定性能的物质是化学服务于人类的责任。解热镇痛药水杨酸改进为阿司匹林、缓释阿司匹林、贝诺酯就是最好的实例。下图表示这三种药物的合成:

(1)反应①的条件是____________;物质B含有的官能团名称是________________
(2)已知乙酸酐是2分子乙酸脱去1分子水的产物,写出M的结构简式__________
(3)反应③的类型____________,写出该反应④的一种副产物的结构简式________
(4)水杨酸与足量Na2CO3溶液能发生反应,写出化学方程式____________________
(5)1mol阿司匹林和1mol缓释长效阿司匹林与NaOH溶液充分反应,最多消耗NaOH的物质的量分别是_________、___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
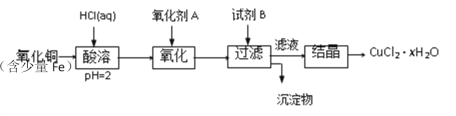
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
(1)加热酸溶过程中发生反应的离子方程式有:______
(2)氧化剂A可选用_______(填编号,下同)
①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用_______
①NaOH ②FeO ③CuO
(4)试剂B的作用是_______
①提高溶液的pH ②降低溶液的pH
③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是___________(按实验先后顺序填编号)
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g。
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g。
试评价上述两种实验方案,其中正确的方案是______,据此计算得x = ______________(用含m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯与乙烷混合气体共a mol,与b mol的氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45 g水。试求:
(1) 当a=1时,乙烯和乙烷的物质的量之比n(C2H4):n(C2H6)=________________________;
(2) 当a=1时,且反应后CO和CO2混合气体的物质的量为反应前氧气的2/3时,则b=_________,得到的CO和CO2的物质的量之比n(CO):n(CO2)=______________。
(3) a的取值范围是____________________;b的取值范围是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知重铬酸根(Cr2O72-)和铬酸根(CrO42-)离子间存在如下平衡:Cr2O72- +H2O ![]() 2CrO42-+2H+。在装有4mL0.1mol·L-1K2Cr2O7溶液中加入1mol·L-1的NaOH数滴,溶液的颜色由_________色变____________色,平衡常数的表达式是 K= __________________________。
2CrO42-+2H+。在装有4mL0.1mol·L-1K2Cr2O7溶液中加入1mol·L-1的NaOH数滴,溶液的颜色由_________色变____________色,平衡常数的表达式是 K= __________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
CO(g)+Cl2(g) ΔH>0,达到平衡时,下列措施:
①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④B.①④⑥C.②③⑤D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化主要形式是___,在导线中电子流动方向为___(用a、b和箭头表示)。
(2)正极反应的电极反应方程式为___。
(3)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。

①图1中N型半导体为___(填“正极”或“负极”)
②该系统工作时,A极的电极反应式为___。
③若A极产生7.00gN2,则此时B极产生___LH2(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com