
用CuFeS2冶炼钢的反应为8CuFeS2+21O2 8Cu+4FeO +2Fe2O3+16SO2.若CuFeS2中Fe的化合价为+2价,下列关于该反应的说法正确的是
8Cu+4FeO +2Fe2O3+16SO2.若CuFeS2中Fe的化合价为+2价,下列关于该反应的说法正确的是
A.CuFeS2只作还原剂
B.Fe元素全部被氧化
C.还原产物是Cu、FeO、Fe2O3和SO2
D.若生成1molCu,则反应中转移2mol电子
C
【解析】
试题分析:A.在反应中CuFeS2中的Cu化合价降低,得到电子,所以CuFeS2作氧化剂,Fe、S的化合价升高,失去电子,作还原剂,因此在反应中CuFeS2既作氧化剂,也作还原剂,错误;B.在反应中,Fe元素一部分价态没有变化,一部分化合价升高,错误;C.在反应中,Cu元素得到电子被还原变为单质Cu,氧气中的氧元素得到电子被还原变为FeO、Fe2O3和SO2,所以还原产物是Cu、FeO、Fe2O3和SO2,正确;D.在氧化还原反应中电子转移数目相等。在该反应中每产生8mol的Cu,转移电子的物质的量是100mol因此若生成1molCu,则反应中转移12.5mol电子,错误。
考点:考查氧化还原反应的物质的作用、概念的辨析、电子转移的知识。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:2014-2015学年上海市黄浦区高三上学期期末调研测试化学试卷(解析版) 题型:选择题
下列表达正确的是
A.氟原子中能量最髙的电子其电子云图:
B.CO2的分子模型示意图:
C.2-甲基丁醛的结构简式:
D.N2的结构式: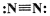
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末考试化学试卷(解析版) 题型:填空题
(本题共12分)氢是宇宙中最丰富的元素,为一切元素之源。
23.H原子的电子排布式是“1s1”,该式子未表明电子运动状态的方面是 (选填编号)。
A.电子层 B.电子亚层
C.电子云的伸展方向 D.电子的自旋
24.金属锂与氢气在一定条件下能直接化合生成 LiH,以下事实能说明LiH是离子化合物的是 (选填编号)。
A.H为-1价 B.熔融状态能导电 C.加热到600℃不分解
LiH的电子式为 。核外有2个电子的简单阴、阳离子有若干种,试比较它们半径的大小 。
25.非金属元素R的气态氢化物的化学式为H8-nR,则R的最高氧化物的化学式为 。
26.根据下表中的键能数据,写出氮气、氢气合成氨气的热化学方程式 。在合成氨的工业生产中,科学家在努力寻找活性温度更低的新催化剂,简述其意义 。
共价键 | 键能(KJ/ mol) |
N≡N | 946 |
H-H | 436 |
H-N | 391 |
27.钯(Pd)是优良的储氢金属:2Pd (s)+xH2(g) 2PdHx (s)?H=-Q(Q>0)
2PdHx (s)?H=-Q(Q>0)
通常状况下,x的最大值为0.8,为使x>0.8可采取的措施是 ;为使PdHx 产生H原子并在固体中快速流动,可采取的措施是 (选填编号)。
A.升温 B.减压 C.及时移走金属钯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末考试化学试卷(解析版) 题型:选择题
以下反应不属于“同一价态的同种元素既被氧化又被还原”的是
A.硫代硫酸钠与稀硫酸 B.硫与热NaOH溶液
C. H2O2溶液中加入MnO2 D.KClO3与盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省安康市高三上学期第二次教学质量调研化学试卷(解析版) 题型:实验题
(12分)实验室利用下列装置可以准备FeCl3(加热、夹持装置和固定装置已略去)。圆底烧瓶中盛装KMnO4,分液漏斗中盛装浓盐酸,B中盛装纯铁粉。已知信息:① FeCl3的熔点为306℃,沸点为315℃。②FeCl3遇水蒸气会产生白雾。请回答下列问题:

(1)检查A装置气密性的操作方法是 。
(2)按气流由左向右流动的方向为A→( )→( )→( )→( )→( )相连进行实验。
(3)C装置的作用是 。
(4)用0.2mol的高锰酸钾固体和足量的浓盐酸完全反应后,得到标准状况下氯气的体积为11.2L,则含锰元素的生成物中锰元素的化合价为 。
(5)写出A装置中发生反应的化学方程式,并标出电子转移的方向和数目 。
(6)检验产品中是否含有FeCl2的实验方案为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省安康市高三上学期第二次教学质量调研化学试卷(解析版) 题型:选择题
在常温常压下,某实验小组按下图做完实验后,实验报告记录如下。其中描述合理的是

A.①②③ B.②③④ C.②⑤⑥ D.③④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山西省晋中市高三1月考前适应性训练理综化学试卷(解析版) 题型:填空题
【化学——物修5:有机化学】氧有机物甲可用来制取多种有用的化工产品,合成路线如下:

已知:
Ⅲ.辛与丁,甲与M分别属于同类物
请回答下列问题:
(1)甲的含氧官能团的名称是 ;写出检验该官能团常用的一种化学试剂的名称和对应的反应条件 。
(2)写出己和丁的结构简式:己 ,丁 。
(3)乙有多种同分异构体,属于甲酸酯,含酚羟基,且酚羟基与酯的结构在苯环邻位的同分异构体共有
种。
(4)在NaOH溶液中发生水解反应时,丁与辛消耗NaOH的物质的量之比为 。
(5)庚与M合成高分子树脂的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省滕州市高三12月月考理综化学试卷(解析版) 题型:选择题
某离子反应涉及H2O、ClO—、IO3—、OH—、I2、Cl—六种微粒。其中c(ClO—)随反应进行逐渐减小。下列判断错误的是
A.该反应的还原剂是I2
B.氧化剂与还原剂的物质的量之比为5:2
C.消耗1 mol氧化剂,转移2 mol电子
D.反应后溶液的碱性明显减弱
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高一上学期第二次月考化学试卷(解析版) 题型:选择题
既能与盐酸反应,又能与NaOH溶液反应的是
①SiO2;②Al(OH)3;③(NH4)2CO3;④Na2CO3;⑤NaHSO3;⑥NaHSO4
A.②③⑤ B.①②③⑥ C.②③④⑤ D.②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com