
分析 (1)根据热化学方程式的书写方法可知,化学计量数与反应热成正比,并注意标明物质的聚集状态,根据燃烧热的概念结合热化学方程式的书写来回答;
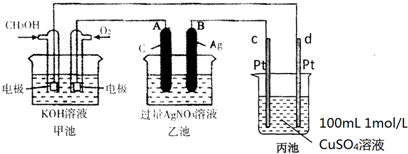
(2)甲池能自发的进行氧化还原反应,属于原电池,通入甲醇的电极为负极、通入氧气的电极为正极,则乙池、丙池是电解池,A、C属于阳极,B、D属于阴极,A电极反应式为氢氧根离子得电子生成氧气,B极反应式为Ag++e-=Ag、C极反应式为4OH-+4e-=2H2O+O2↑、D极反应式为Cu2++2e-=Cu,据此分析解答;
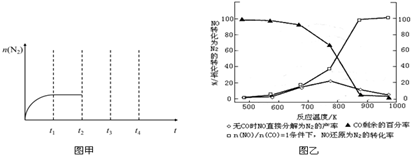
(3)①平衡状态时正逆反应速率相等,各组分的浓度保持不变;
②要提高CO的转化率,应使平衡向正反应方向移动,结合化学平衡移动原理分析选项.
解答 解:(1)32gCH3OH在氧气中燃烧生成CO2和液态水,放出726.4kJ热量,64g即2molCH3OH在氧气中燃烧生成CO2和液态水,放出1452.8kJ热量,
则燃烧热的热化学方程式为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8 kJ•mol-1,
故答案为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452.8 kJ•mol-1;
(2)①甲池能自发的进行氧化还原反应,属于燃料电池,为原电池,通入甲醇的电极为负极、通入氧气的电极为正极,乙为电解池,A连接原电池正极,则为阳极,
故答案为:阳极;
②碱性条件下,氧气得电子生成氢氧根离子,电极反应式为O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-;
③碱性条件下,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O,
故答案为:CH3OH+8OH--6e-=CO32-+6H2O;
④乙池为电解硝酸银溶液的电解池,生成Ag和氧气,电解方程式为4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O$\frac{\underline{\;通电\;}}{\;}$4Ag+O2↑+4HNO3;
⑤丙池中C极反应式为4OH-+4e-=2H2O+O2↑、D极反应式为Cu2++2e-=Cu,当电路中通过0.01mol电子时,有0.01mol氢氧根离子反应,生成0.01mol氢离子,所以c(H+)=$\frac{0.01mol}{0.1L}$=0.1mol/L,故答案为:0.1;
(3)①a.容器体积不变,混合气体的质量不变,所以密度始终不变,混合气体的密度保持不变不能说明反应达到平衡状态,故a错误;
b.该反应前后气体物质的量不同,恒容容器中混合气体的总压强保持不变,说明各组分浓度不变,反应达到平衡状态,故b正确;
c.CO的质量分数保持不变,说明反应达到平衡状态,故c正确;
d.甲醇的浓度保持不变,说明反应达到平衡状态,故d正确;
e.氢气以甲醇的化学计量数不同,v正(H2)=v逆(CH3OH),不能说明正逆反应速率相等,不能说明反应达到平衡状态,故e错误;
f.v(CO)=v(CH3OH),无法判断正逆反应速率相等,故f错误;
故答案为:bcd;
②要提高CO的转化率,应使平衡向正反应方向移动,
a.该反应放热,升温平衡逆向移动,故错误;
b.加入催化剂不影响平衡移动,故错误;
c.增加CO的浓度,CO的转化率降低,故错误;
d.加入H2平衡正向移动,CO的转化率增大,故正确;
e.体积不变加入惰性气体,平衡不移动,故错误;
f.分离出甲醇平衡正向移动,CO的转化率增大,故正确;
故答案为:df.
点评 本题考查了热化学方程式书写、原电池电解池相关知识、化学平衡的移动以及转化率大小的判断,题目综合性强,难度较中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=-2 878 kJ•mol-1 | B. | △H=-2 658 kJ•mol-1 | ||
| C. | △H=-1 746 kJ•mol-1 | D. | △H=-1 526 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
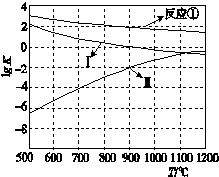 用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术.反应①为主反应,反应②和③为副反应.
用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术.反应①为主反应,反应②和③为副反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl 和 NaOH 反应的中和热△H=-57.3 kJ/mol,则浓 H2SO4和 Ca(OH)2反应的中和热 △H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是 283.0 kJ/mol,则 2CO2(g)═2CO(g)+O2(g)反应的△H=2×283.0 kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X的反应速率为0.2 mol•L-1•s-1,则Z的反应速率为0.3 mol•L-1•s-1 | |
| B. | 若向容器中充入氦气,压强增大,Y的转化率提高 | |
| C. | 升高温度,正反应速率减小,平衡向逆反应方向移动 | |
| D. | 开始充入容器中的X、Y物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电源B 极的名称是负极 | |
| B. | 甲装置中电解反应的总化学方程式是:CuSO4+Fe$\frac{\underline{\;电解\;}}{\;}$Cu+FeSO4 | |
| C. | 设电解质溶液过量,则同一时内C、D电极上参加反应的单质或生成的单质的物质的量之比是1:1 | |
| D. | 设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为0.2mol/L. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com