
 图是最简单的铜-锌原电池.对于该原电池,下列说法中不正确的是( )
图是最简单的铜-锌原电池.对于该原电池,下列说法中不正确的是( )| A、①②③ | B、③④⑤ |
| C、①②⑥ | D、④⑤⑥ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| W | X | |
| Y | Z |
| A、X、Y、Z中最简单氢化物稳定性最弱的是Y |
| B、Z元素氧化物对应水化物的酸性一定强于Y |
| C、X元素形成的单核阴离子还原性强于Y |
| D、Z元素单质在化学反应中只表现氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过量氨气通入Al2(SO4)3溶液 |
| B、过量CO2通入CaCl2溶液 |
| C、少量SO2通入BaCl2溶液后再通入过量Cl2 |
| D、过量CO2通入Na2SiO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、太阳能、核能和天然气都属于新型能源 |
| B、哥本哈根气候大会讨论的减排目标主要是控制二氧化硫排放 |
| C、84消毒液具有强氧化性,可杀死流感病毒 |
| D、比黄金还贵的18O2和普通的16O2是两种不同的核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
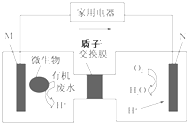 有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机废水的化学能直接转化为电能,该装置的构造如图所示.下列说法中正确的是( )
有媒体报道一种新型污水处理装置问世,该装置可利用一种微生物将有机废水的化学能直接转化为电能,该装置的构造如图所示.下列说法中正确的是( )| A、装置外电路中箭头的方向代表电流的方向 |
| B、该装置为原电池装置,其中N为负极 |
| C、若有机废水中含有葡萄糖,则M电极发生的电极反应式为C6H12O6+6H2O-24e-═6CO2+24H+ |
| D、该处理工艺会导致有机废水酸性增强,仍旧不能直接排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、488.3 kJ/mol |
| B、-488.3 kJ/mol |
| C、-244.15 kJ/mol |
| D、244.15 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10L 0.05mol?L-1Ba(OH)2溶液与20L0.05mol?L-1HNO3反应时的反应热是中和热 |
| B、1molHCl气体通入1L 0.01mol?L-1NaOH溶液中反应时的反应热是中和热 |
| C、1molHClO与2molNaOH溶液反应时的反应热也可能是中和热 |
| D、只要强酸与强碱在衡溶液中反应生成1mol水时的反应热就是中和热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com