
某矿石含碳酸镁和石英,制备高纯硅和硅胶的工艺流程如下:
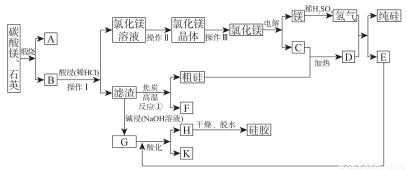
(1)“硅胶”冶常用作_______________ ,也可以用作__________的载体。 A 的结构式为________。
(2)制备粗硅的方程式为_______。
(3)操作I为_____________,操作Ⅱ为_______________,操作Ⅲ所用仪器有铁架台(带铁圈)、酒精灯、_______________等。
(4)操作Ⅲ,需要在氯化氢气流中加热脱水的原因是_______________。
(5)溶液G用E酸化的方程式为_______________。
(6)电解饱和的K溶液的离子方程式为____________,阳极电极方程式为_______________。
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为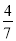 计算:
计算:
(1)该条件下N2的平衡转化率;(小数点后保留一位)
(2)该条件下反应2NH3(g) N2(g)+3H2(g)的平衡常数。(不带单位)
N2(g)+3H2(g)的平衡常数。(不带单位)
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟九化学试卷(解析版) 题型:填空题
某同学所做的有关铜元素的实验流程如图:

(1)写出基态铜原子的价电子排布式________________________,向深蓝色溶液中加入适量乙醇,会析出深蓝色晶体,该晶体中存在的化学键的类型有________________________。
(2)写出反应④的离子方程式________________________。
(3)铜能与类卤素(SCN) 2反应生成Cu(SCN) 2,1 mol (SCN)2分子中含有的δ键数目为类卤素(SCN)2 对应的酸有两种,理论推测硫氰酸(H-S-C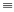 N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是__________________;写出一种与SCN-互为等电子体的分子_________________(用化学式表示)。
N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是__________________;写出一种与SCN-互为等电子体的分子_________________(用化学式表示)。
(4)氨基乙酸铜的分子结构如图,碳原子的杂化方式为____________________。
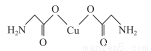
(5)铜晶胞中,其晶体的堆积方式为_______________,一个晶胞中铜原子的数目为__________,空间利用率为____________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟九化学试卷(解析版) 题型:选择题
下列说法正确的是
A.CO(g)的燃烧热:△H=-283.0KJ/ mol,则 2CO2(g ) =2CO(g)+O2(g)反应的△H= -55.0KJ/ mol
B.已知NaOH(aq) +HCl(aq )= NaCl(aq) +H2O(l) △H = -57.30KJ/ mol-1 ,则含40.0gNaOH的稀溶液与稀醋酸完全中和,放出57.3KJ的热量
C.已知2C(s)+2O2(g)=2CO2 (g) △H=a;2C(s)+O2 (g )=2CO(g) △H=b;则a>b
D.已知c(石墨,s)= C(金刚石,s) △H>0,则石墨比金刚石稳定
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟八化学试卷(解析版) 题型:选择题
分析原子的杂化方式,并根据等电子体原理判断下列各组分子中的所有原子,或者处于同一平面,或者在一条直线上的是( )
A.C2H2、HClO、C2H6 B.CO2、N2O、HC≡CH
C.C6H5CH3、C3H4、CH4 D.C6H6、C2H4、HCN
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟八化学试卷(解析版) 题型:选择题
神舟十号飞船,神舟飞船的统一双组元,推进系统采用肼作为燃料,简化了增压系统的设计,工作更为可靠。 肼——空气燃料电池是一种碱性燃料电池,电解质溶液是20% ~ 30%的KOH 溶液,总反应式为N 2H4+O2=N2+2H2O,下列说法中,错误的是
A.该电池放电时,通入肼的一极为负极
B.电池每释放1molN2转移的电子数为4NA
C.电池工作一段时间后,电解质溶液的pH将不变
D.通入空气的一极的电极反应式是:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟八化学试卷(解析版) 题型:选择题
下列有关物质的性质与应用不相对应的是
A. 氨气能与氯气生成氯化铵,可用浓氨水检验输送氯气的管道是否泄漏
B.SO2有强还原性,用 SO2漂白纸浆
C.熟石膏与水的糊状混合物会很快凝固,可用它制作模型和石膏绷带
D.铝有强还原性且转化为氧化铝时放出大量的热,可用铝粉来还原某些金属氧化物
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三5月月考理综化学试卷(解析版) 题型:简答题
【化学——选修化学与技术】铝是一种重要的金属,在生产、生活中具有许多重要的用途,如下框图是从铝土矿中制备铝的工艺流程:

已知:①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学方程式为:2Na2SiO3+2NaAlO2+4H2O=Na2Al2Si2O8↓+2H2O+4NaOH
回答下列问题:
(1)溶解铝土矿时,发生反应的离子方程式为:____________。
(2)滤渣A的主要成分________;硅铝酸盐沉淀写成氧化物的形式是________。
(3)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是 _。
(4)若该工厂用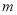 kg铝土矿共制得
kg铝土矿共制得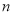 kg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
kg Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为______。
(5)若将铝溶解,下列试剂中最好选用_____ __(填编号)。
A.浓硫酸B. 稀硫酸C.稀HNO3 D.浓HNO3
(6)电解冶炼铝时用Na3AlF6作助熔剂, Na3AlF6是配合物,其中内界是___,配位数为_ ____。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江双鸭山一中高二下期中化学试卷(解析版) 题型:选择题
由乙炔、苯和甲醛组成的混和物中,测得含碳元素的质量百分含量为72%,则混和物中氧元素的质量百分含量为( )
A 22% B 20.7% C 28% D 24.9%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com