
| A. | 白醋中滴入石蕊试液呈红色 | |
| B. | 白醋加入豆浆中有沉淀产生 | |
| C. | 经检验白醋中c(H+)约为0.01 mol•L-1 | |
| D. | 蛋壳浸泡在白醋中有气体放出 |
分析 A.酸遇紫色的石蕊变红属于酸的通性,无法证明醋酸部分电离;
B.白醋加入豆浆中产生沉淀,只能说明白醋是电解质,但无法证明醋酸在水溶液里的电离程度;
C.根据酸的电离的程度来分析醋酸为弱电解质;
D.醋酸的酸性大于碳酸,应用碳酸为弱酸,则无法证明醋酸为弱酸.
解答 解:A.白醋中滴入石蕊试液呈红色,说明白醋为酸,但不能说明醋酸部分电离,所以不能证明醋酸为弱电解质,故A错误;
B.白醋加入豆浆中产生沉淀,说明白醋是电解质,但不能说明醋酸在水溶液里部分电离,所以不能证明醋酸是弱电解质,故B错误;
C.1mol/L的白醋中c(H+)=0.01 moL/L<1mol/L,则说明白醋部分电离,则证明醋酸是弱电解质,故C正确;
D.蛋壳浸泡在白醋中有气体放出,说明醋酸的酸性大于碳酸,但不能说明醋酸部分电离,则不能证明醋酸是弱电解质,故D错误;
故选C.
点评 本题考查了弱电解质的电离平衡及其应用,题目难度中等,注意根据电离程度确定电解质强弱,不能根据物质的溶解性大小、溶液酸碱性判断电解质强弱,试题培养了学生的灵活应用能力.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 1H和3H是不同的核素 | |
| B. | 1H、2H、3H、H+和H2是氢元素的五种不同粒子 | |
| C. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 | |
| D. | 石墨和金刚石互为同位素,化学性质相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由氢氟酸刻蚀玻璃可推知盐酸也能用来刻蚀玻璃 | |
| B. | 由Na20中阴阳离子个数比为1:2,可推知Na202中阴阳离子个数比为1:1 | |
| C. | 由铁和溴反应生成溴化铁,可推知铁和碘单质反应生成碘化铁 | |
| D. | 由钠与冷水剧烈反应,可推知钾也能与冷水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
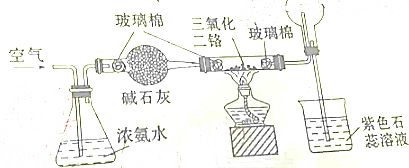
| A. | 烧杯中的紫色石蕊溶液不变色 | |
| B. | 圆底烧瓶中的气体一定为无色 | |
| C. | 加热后,通过三氯化二铬的气体由无色变为红棕色 | |
| D. | 三氯化二铬起氧化剂的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 生成白色沉淀 |
| ② | A+C | 放出无色气体 |
| ③ | A+D | 放出无色气体 |
| ④ | B+C | 无明显变化 |
| ⑤ | B+D | 生成白色沉淀 |
| ⑥ | C+D | 无明显变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com