
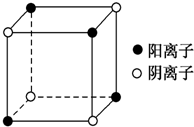
 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1.请回答下列问题:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1.请回答下列问题:分析 A、B、C、D四种元素,B原子得一个电子后3p轨道全满,则B是Cl元素;A+比B-少一个电子层,则A是Na元素;C原子的p轨道中有3个未成对电子,则为第VA族元素,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,说明其氢化物中能和水形成分子间氢键,所以C是N元素;D的最高化合价和最低化合价的代数和为4,处于ⅥA族,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数,所以D是S元素;R是由A、D两元素形成的离子化合物,其中A与D离子的数目之比为2:1,则R是Na2S,据此解答.
解答 解:A、B、C、D四种元素,B原子得一个电子后3p轨道全满,则B是Cl元素;A+比B-少一个电子层,则A是Na元素;C原子的p轨道中有3个未成对电子,则为第VA族元素,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大,说明其氢化物中能和水形成分子间氢键,所以C是N元素;D的最高化合价和最低化合价的代数和为4,处于ⅥA族,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数,所以D是S元素;R是由A、D两元素形成的离子化合物,其中A与D离子的数目之比为2:1,则R是Na2S.
(1)A单质、B单质、化合物R分别是Na、Cl2、Na2S,硫化钠是离子晶体,钠是金属晶体,固体氯气是分子晶体,金属Na的熔点很低,故晶体熔点高低顺序是:R>A单质>B单质,故选②;
(2)NCl3分子中氮原子含有3个共价单键且含有一个孤电子对,其固态时的晶体中构成微粒是分子,所以晶体类型为分子晶体,
故答案为:分子晶体;
(3)D是S元素,原子的核外电子排布式1s22s22p63s23p4,C的氢化物是NH3,D的氢化物是H2S,氨气分子和水分子间能形成氢键且能发生化学反应,导致氨气溶解性大于硫化氢,
故答案为:1s22s22p63s23p4;氨气分子和水分子间能形成氢键且能发生化学反应;
(4)FeS2晶体中阴离子数目为4×$\frac{1}{8}$=$\frac{1}{2}$、阳离子数目为4×$\frac{1}{8}$=$\frac{1}{2}$,故阴离子、阳离子数之比为1:1,FeS2物质中含有离子键,S22-含有共价键,
故答案为:1:1;离子键、共价键.
点评 本题是对物质结构和性质的考查,涉及晶体类型、熔沸点比较、核外电子排布、氢键、化学键、晶胞计算等,正确推断元素是解本题关键,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制快速氨气可用浓氨水滴加到固体NaOH中 | |
| B. | 漂白粉的成分是NaCl与NaClO | |
| C. | 水玻璃应保存在具橡皮塞的玻璃试剂瓶中 | |
| D. | NO气体的收集不能用排空气法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素 | Al | B | Be | C | Cl | F | Li |
| X的数值 | 1.5 | 2.0 | 1.5 | 2.5 | 2.8 | 4.0 | 1.0 |
| 元素 | Mg | Na | O | P | S | Si | |
| X的数值 | 1.2 | 0.9 | 3.5 | 2.1 | 2.5 | 1.7 |
| C--C | C--N | C--S | |
| 键能 KJ/mol | 347 | 305 | 259 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
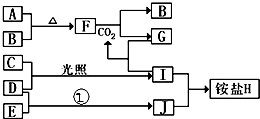 如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种固氮反应.
如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种固氮反应. .
. 2NH3的化学方程式.
2NH3的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BeF2分子中,中心原子Be的价层电子对数等于2,其空间排布为直线,成键电子对数也等于2 | |
| B. | BeF2分子的立体结构为直线形 | |
| C. | SF2分子中,中心原子S的价层电子对数等于4,其空间排布为四面体,成键电子对数等于2,没有孤对电子 | |
| D. | 在气相中,BeF2是直线形而SF2是V形 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中由水电离的c(H+)<10-7mol/L | |
| B. | 该溶液由0.1mol/L的CH3COOH溶液与等物质的量浓度等体积的NaOH溶液混合而成 | |
| C. | 该溶液由V1L c mol/L的CH3COOH溶液与V2Lc mol/L的NaOH溶液混合而成,且V1<V2 | |
| D. | 在上述溶液中加入适量NaOH,可使溶液中离子浓度改变为:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com