


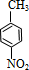
 ,甲氧化生成乙为
,甲氧化生成乙为 ,乙与E发生酯化反应生成
,乙与E发生酯化反应生成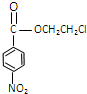 ,则E为HOCH2CH2Cl,
,则E为HOCH2CH2Cl,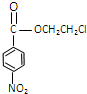 与氢气反应还原硝基变为氨基,丙为
与氢气反应还原硝基变为氨基,丙为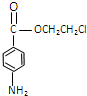 ,丙与F发生取代反应生成普鲁卡因,然后结合物质的性质来解答.
,丙与F发生取代反应生成普鲁卡因,然后结合物质的性质来解答. ,甲氧化生成乙为
,甲氧化生成乙为 ,乙与E发生酯化反应生成
,乙与E发生酯化反应生成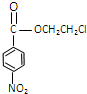 ,则E为HOCH2CH2Cl,
,则E为HOCH2CH2Cl,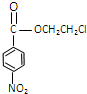 与氢气反应还原硝基变为氨基,丙为
与氢气反应还原硝基变为氨基,丙为 ,丙与F发生取代反应生成普鲁卡因,
,丙与F发生取代反应生成普鲁卡因, ,由甲苯生成甲的反应类型是取代反应,
,由甲苯生成甲的反应类型是取代反应, ;取代反应;
;取代反应; ,官能团为羧基、硝基,反应③的化学方程式为:
,官能团为羧基、硝基,反应③的化学方程式为: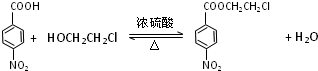 ,
, ;
; ,含有的官能团有:氯原子、酯基、氨基,
,含有的官能团有:氯原子、酯基、氨基, ,故答案为:
,故答案为: ;
; ,
, .
.


科目:高中化学 来源: 题型:
| A、邻二甲苯可作生产D的原料 |
| B、E可发生银镜反应 |
| C、E可与FeCl3发生显色反应 |
| D、F与D的相对分子质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 (其中I、Ⅱ为未知部分的结构)为推测X的分子结构,进行如图的转化:
(其中I、Ⅱ为未知部分的结构)为推测X的分子结构,进行如图的转化:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、麦芽糖属于还原型二糖 |
B、一种塑化剂的结构为 ,该物质属于油脂 ,该物质属于油脂 |
| C、氨基酸是两性化合物,能与酸、碱反应生成盐 |
| D、用浸泡过高锰酸钾溶液的硅土吸收水果释放出的乙烯,可达到水果保鲜的目的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com