
【题目】右图为电解稀Na2SO4水溶液的装置,通电后,石墨两极附近分别滴加几滴酚酞溶液,下列有关说法不正确的是

A.a电极附近呈红色, b电极附近无明显变化
B.逸出气体的体积,a电极的大于b电极的
C.Na2SO4水溶液浓度逐渐增大
D.当电路中通过0.04mol e-时,a电极逸出气体的体积为448mL
科目:高中化学 来源: 题型:
【题目】用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
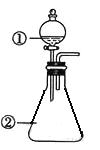
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A. | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B. | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C. | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D. | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人认为人体实际上是一架缓慢氧化着的“高级机器”,人体在生命过程中也需要不断的补充“燃料”。按照这种观点,你认为人们通常摄入的下列物质不能看作“燃料”的是( )
A. 油脂 B. 蛋白质 C. 水 D. 葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的说法正确的是( )
A.原电池将化学能转变为电能
B.原电池将电能转变为化学能
C.中和反应放热说明中和反应前后能量不守恒
D.吸热反应中生成物的总能量低于反应物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,4 g H2含有的分子数为 2NA
B.8 g H2O在标准状况下的体积是22.4 L
C.2.3 g金属钠变为钠离子时失去的电子数为NA
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物种类繁多的原因,不正确的是( )
A. 碳原子有四个价电子
B. 碳原子彼此可结合成长链或各种环状
C. 组成有机物的元素种类很多
D. 有机物容易形成同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】量取100 mL碘的饱和水溶液,倒入分液漏斗中,然后再注入4 mL四氯化碳,用力振荡后静置,实验现象为
A. 液体分层,上层为四氯化碳层,黄色 B. 液体分层,上层为水层,紫色
C. 液体分层,下层为四氯化碳层,紫色 D. 液体分层,下层为水层,黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置,电解质溶液均为足量,回答下列问题

(1)电极名称:Cu电极 极,甲池发生的电极总反应离子方程式
(2)若用U形铜丝代替“盐桥”,工作一段时间后,甲池中Ag电极质量增加5.4g时,乙池电解质溶液为饱和食盐水。乙池中电极总反应化学方程式 ;
U形铜丝反应前后质量变化 (填写增大、减小、不变);若要恢复乙池电解质溶液浓度、体积,需向溶液中加 (填物质名称)物质的量为 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

①由图1可知SCR技术中的氧化剂为: 。
②图2是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知最佳的催化剂和相应的温度分别为: 。
③用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图3所示,脱氮效果最佳的c(NO2)/c(NO)= 。已知生成1 mol N2反应放出的热量为Q kJ,此时对应的脱氮反应的热化学方程式为 。

(2)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,具体步骤如下:
SO2(g)+H2O(l)H2SO3(l)H+(aq)+HSO![]() (aq) Ⅰ
(aq) Ⅰ
HSO![]() (aq) H+(aq)+SO
(aq) H+(aq)+SO![]() (aq) Ⅱ
(aq) Ⅱ
Ca(OH)2(s) Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+SO![]() (aq) CaSO3(s) Ⅳ
(aq) CaSO3(s) Ⅳ
④步骤Ⅱ的平衡常数K的表达式为 。
⑤该温度下,测定吸收后液体中c(Ca2+)一直保持为0.70 mol/L,已知Ksp(CaSO3)=1.4×10-7,试计算吸收后溶液中的SO![]() 的浓度。(写出计算过程)
的浓度。(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com