
【题目】H2和CO是合成许多有机物的原料,有如下反应:mH2+nCO==wX(反应条件已省去,m、n、w为化学计量数)。如m:n=l:1且w=l,则有机物X可能是①HCHO②C2H5OH ③CH3COOH ④CH3CHO 中的
A. ①和② B. ①和③ C. ②和③ D. ①和④
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
请回答:
(1)沉淀a中含有的单质是;
(2)沉淀b的化学式是;
(3)沉淀c的化学式是;
(4)溶液A与H2O2溶液在酸性条件下反应的离子方程式是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①镧系合金是稀土系储氢合金的典型代表,由荷兰菲利浦实验室首先研制出来。它的最大优点是容易活化,其晶胞结构如图所示。 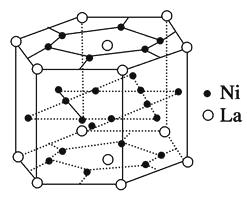
它的化学式为。
②镁系合金是最早问世的合金之一,经X射线衍射实验分析得镁铜合金为面心立方结构,镁镍合金为六方最密堆积。镁系合金的优点是价格较低,缺点是要加热到250℃以上时才释放出氢气。下列有关说法不正确的是
A.金属铜的晶胞结构为 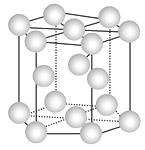
B.已知钛和镁的堆积方式相同,均为六方最密堆积,则其堆积方式为 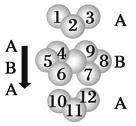
C.镁铜合金晶体的原子空间利用率为74%
D.镁镍合金晶体的配位数为12
③《X射线金相学》中记载关于铜与金可形成两种有序的金属互化物,其结构如图。下列有关说法正确的是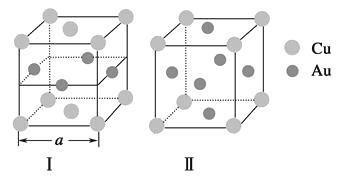
A.图Ⅰ、Ⅱ中物质的化学式相同
B.图Ⅱ中物质的化学式为CuAu3
C.图Ⅱ中与每个铜原子紧邻的铜原子有3个
D.设图Ⅰ中晶胞的边长为acm,则图Ⅰ中合金的密度为 ![]() g·cm-3
g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应的本质的说法正确的是( )
A.化学反应都有新物质生成
B.化学反应都有能量变化
C.化学反应是旧键断裂新键形成的过程
D.化学反应的发生都需要在一定条件下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在恒温条件下,将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):。
(2)0~10min化学反应速度V(X)=。
(3)比较Y在0~10min和10~20min时平均反应速率的大小:v(0~10) v(10~20)(填“<”、“>”或“=”),原因是。
(4)a、b、c、d四个点中,表示化学反应处于平衡状态的点是 , 理由是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国化学家鲍林教授具有独特的化学想象力:只要给他物质的分子式,他就能大体上想象出这种物质的分子结构模型.多核离子所带电荷可以认为是中心原子得失电子所致,根据VSEPR模型,下列离子中所有原子都在同一平面上的一组是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】存在于自然界的植物中,其K1=5.4×10﹣2 , K2=5.4×10﹣5 . 草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O42H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解.请回答下列问题: 
(1)甲组同学按照图1所示装置,通过实验检验草酸晶体的分解产物.装置C中可观察到的现象是 , 由此可知草酸晶体分解的产物中有 . 装置B的主要作用是 .
(2)乙组同学认为草酸晶体分解产物中还有CO,为进行验证,选用甲组实验中的装置A、B和如图所示的部分装置(可以重复选用)进行实验. 
① 乙组同学的实验装置中,依次连接的合理顺序为A、B、 . 装置H反应管中盛有的物质是 .
②能证明草酸晶体分解产物中有CO的现象是 .
(3)设计实验证明: ①草酸的酸性比碳酸的强 .
②草酸为二元酸 .
(4)草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4溶液、MnO2氧化,锰元素被还原为+2价.KMnO4溶液和草酸钠溶液在稀硫酸中反应的离子方程式为: . 实验室常用固体草酸钠测定KMnO4溶液的浓度.准确称取0.2000g草酸钠,放入锥形瓶中,加入100mL稀硫酸溶解,用配制好的KMnO4溶液滴定,三次重复实验消耗KMnO4溶液的体积分别是16.02mL、16.00mL、16.01mL,则KMnO4溶液的物质的量浓度的计算式是:c(KMnO4)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有原子序数小于20的A、B、C、D、E、F6种元素,它们的原子序数依次增大,已知B元素是地壳中含量最多的元素;A和C的价电子数相同,B和D的价电子数也相同,且A和C两元素原子核外电子数之和是B、D两元素原子核内质子数之和的;C、D、E三种元素的基态原子具有相同的电子层数,且E原子的p轨道上电子数比D原子的p轨道上多一个电子;6种元素的基态原子中,F原子的电子层数最多且和A处于同一主族。回答下列问题:
(1)用电子式表示C和E形成化合物的过程。
(2)写出基态F原子的核外电子排布式。
(3)写出A2D的电子式 , 其分子中(填“含”或“不含”,下同)σ键,π键。
(4)A、B、C共同形成的化合物中化学键的类型有。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W,X,Y,Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料.Z的非金属性在同周期元素中最强.下列说法正确的是( ) 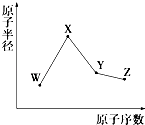
A.对应简单离子半径:X>W
B.对应气态氢化物的稳定性:Y>Z
C.化合物XZW既含离子键,又含共价键,属于弱电解质
D.Y的氧化物和Z的氢化物均能与X的最高价氧化物对应的水化物反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com