
A、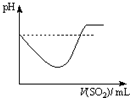 |
B、 |
C、 |
D、 |


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
| A、①② | B、③④ | C、③⑤ | D、①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a、b两处均有颜色变化,证明单质氧化性:CI2>Br2>I2 |
| B、c处先变红,后褪色,证明氯气与水反应生成了酸性物质 |
| C、d处立即褪色,证明氯气与水反应生成了漂白性物质 |
| D、e处变红色,证明氧化性:C12>Fe3+,还原性:Cl-<Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、石灰石与盐酸反应:C
| ||
| B、醋酸与烧碱溶液反应:H++OH-═H2O | ||
| C、氧化铜与盐酸反应:O2-+2H+═H2O | ||
| D、硫酸与氨水混合:H++NH3?H2O═NH4++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O2+共有11个核外电子 |
| B、化合物中含有离子键、极性共价键、非极性共价键 |
| C、化合物O2ASF6中AS的化合价为+5价 |
| D、化合物O2ASF6为离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 25 |
| 2 |
| A、H2 |
| B、CO |
| C、C8H18 |
| D、CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对废旧电池进行回收处理,主要是为了环境保护和变废为宝 |
| B、用电解水的方法制取大量H2,可以缓解能源不足的问题 |
| C、大力开发和应用氢能源有利于实现“低碳经济” |
| D、工业上,不能采用电解MgCl2溶液的方法制取金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3+H2O=H2SO4 | ||||
| B、CaCO3+2HCl=CaCl2+H2O+CO2↑ | ||||
| C、Cl2+H2O=HCl+HClO | ||||
D、2NaHCO3
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com