
 2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为 。
2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为 。  Ca2SiO4 (l) + 2Mg(g)
Ca2SiO4 (l) + 2Mg(g) 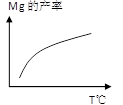
 Ca2SiO4 (l) + 2Mg(g)
Ca2SiO4 (l) + 2Mg(g) 

科目:高中化学 来源:不详 题型:填空题
 2SO3(g)
2SO3(g) 2SO3(g),化学平衡状态的标志为__________。
2SO3(g),化学平衡状态的标志为__________。| A.SO2减少的化学反应速率和SO3减少的化学反应速率相等 |
| B.容器中气体的平均分子量不随时间而变化 |
| C.容器中气体的分子总数不随时间而变化 |
| D.恒容的容器中气体的密度不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 B(g)+C(g)。若反应物的浓度由3 mol·L-1降到1.8 mol·L-1需30 s,那么反应物浓度由0.8 mol·L-1降至0.2 mol·L-1所需反应时间为( )
B(g)+C(g)。若反应物的浓度由3 mol·L-1降到1.8 mol·L-1需30 s,那么反应物浓度由0.8 mol·L-1降至0.2 mol·L-1所需反应时间为( )| A.15 s | B.大于15 s | C.小于15 s | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
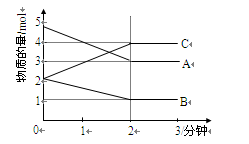
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3,在5 min内,N2的物质的量浓度由6 mol / L,变为2 mol / L,则用NH3表示该反应在这段时间的平均速率为
2NH3,在5 min内,N2的物质的量浓度由6 mol / L,变为2 mol / L,则用NH3表示该反应在这段时间的平均速率为 | A.4 mol / (L?min) | B.1.6 mol / (L?min) |
| C.0.8 mol / (L?min) | D.0.6 mol / (L?min) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L,对此反应速率的表示不正确的是( )
2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L,对此反应速率的表示不正确的是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
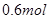 气体X和
气体X和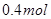 气体Y混合于2L容器中,发生反应:
气体Y混合于2L容器中,发生反应: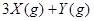
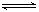
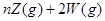 ,5分钟末已生成
,5分钟末已生成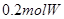 ,若测知以Z浓度变化来表示的平均速率为
,若测知以Z浓度变化来表示的平均速率为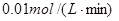 ,则:
,则:| A.20% | B.25% | C.33% | D.50% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com