
【题目】某三原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏加德罗常数为NA , 则:
(1)该气体在标准状况下的体积为 ________ L.
(2)该气体在标准状况下的密度为 ________ g/L.
(3)该气体所含原子总数为 ________ 个.
(4)该气体的一个分子的质量为 ________ g.
(5)该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________mol/L
【答案】 ![]()
![]()
![]()
![]()
![]()
【解析】
(1)根据n=![]() 计算出该气体的物质的量,再根据V=nVm计算出气体的体积;(2)根据M=ρVm计算出气体的密度;(3)根据n=
计算出该气体的物质的量,再根据V=nVm计算出气体的体积;(2)根据M=ρVm计算出气体的密度;(3)根据n=![]() 计算出该气体的物质的量,再根据N=nNA计算出含有的原子数;(4)根据摩尔质量为M、阿伏伽德罗常数NA计算出该气体的一个分子的质量;(5)根据n=
计算出该气体的物质的量,再根据N=nNA计算出含有的原子数;(4)根据摩尔质量为M、阿伏伽德罗常数NA计算出该气体的一个分子的质量;(5)根据n=![]() 计算出该气体的物质的量,再根据c=
计算出该气体的物质的量,再根据c=![]() 计算出溶液的物质的量浓度。
计算出溶液的物质的量浓度。
(1)该气体的物质的量为:n=![]() =
=![]() mol,标况下气体的体积为:22.4L/mol×
mol,标况下气体的体积为:22.4L/mol×![]() mol=
mol=![]() L;(2)根据M=ρVm可知,标况下该气体的密度为:ρ=
L;(2)根据M=ρVm可知,标况下该气体的密度为:ρ=![]() =
=![]() g/L;(3)该气体的物质的量为:n=
g/L;(3)该气体的物质的量为:n=![]() =
=![]() mol,该气体分子含有3个原子,则含有的原子的物质的量为:
mol,该气体分子含有3个原子,则含有的原子的物质的量为:![]() mol×3=
mol×3=![]() mol,含有的原子数为:
mol,含有的原子数为:![]() ×NA=
×NA=![]() ;(4)该气体的一个分子的质量为:
;(4)该气体的一个分子的质量为:![]() =
=![]() g;(5)mg该气体的物质的量为:n=
g;(5)mg该气体的物质的量为:n=![]() =
=![]() mol,该气体完全溶于水形成VL溶液,溶液的物质的量浓度为:c=
mol,该气体完全溶于水形成VL溶液,溶液的物质的量浓度为:c=![]() =
=![]() mol/L。
mol/L。


科目:高中化学 来源: 题型:
【题目】已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O,其中1mol氧化剂在反应中得到的电子为( )
A.10mol
B.11mol
C.12mol
D.13mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.材料的不断发展可以促进社会进步.
(1)钢铁是制造航母的主要材料,钢铁在潮湿空气中易发生________ 腐蚀,其负极反应是________ .请列举一种防止钢铁腐蚀的方法:________ .
(2)不锈钢丝与棉纤维可织成一种防辐射布料.这种布料属于________ (填字母).
a.合金材料 b.复合材料 c.陶瓷材料
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机.请写出高纯硅和氮气在1300℃时反应制备氮化硅的化学方程式:________ .
II.我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
(1)往燃煤中加入________ (填化学式),可大大减少产物中的SO2 .
(2)漂白粉用于生活用水的杀菌消毒,漂白粉的有效成份是________ (填化学式).治理废水中的重金属污染物可用沉淀法.例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为________ (填化学式)沉淀而除去.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质实验的叙述,正确的是
A.钠在空气中燃烧,生成淡黄色的氧化钠
B.钠是一种强还原剂,可以把钛从其盐溶液中置换出来
C.将灼热的铜丝放入盛有氯气的集气瓶中,生成棕黄色的雾
D.Fe(OH)3胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可用于净水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O ,下列哪一种物质能使上述还原过程发生( )
A.KMnO4B.Na2CO3C.Cu2OD.Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种有机光电材料中间体,由A制备F的一种合成路线如下:

已知:![]()
回答下列问题:
(1)A的结构简式为________,C的化学名称是______。
(2)①、③的反应类型分别是______、_______。
(3)②的反应条件是_______,有机物X的结构简式为____________。
(4)反应⑤的化学方程式为___________________。
(5)芳香化合物H是D的同分异构体,满足下列条件的同分异构体共有____种;
a.能发生银镜反应 b.含有—C≡CH结构 c.无—C≡C—O—结构
写出其中核磁共振氢谱峰面积比为1:2:2:1的一种有机物的结构简式_______。
(6)写出由1-丁炔和乙炔为原料制取化合物 的合成略线(其他试剂任选)_____。
的合成略线(其他试剂任选)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5 mol,K+和Na+共1.5 mol,Mg2+为0.5 mol,则SO42-的物质的量为( )
A.1 molB.0.5 molC.0.25 molD.0.15 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠的工艺流程如下:
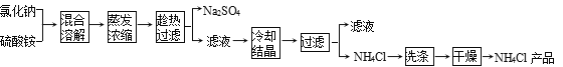
【查阅资料】
①上述流程所示物质中只有NH4Cl受热易分解:NH4Cl![]() NH3↑+HCl↑
NH3↑+HCl↑
②氯化铵和硫酸钠的溶解度随温度变化曲线如下图所示:
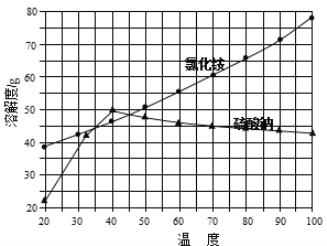
请回答下列问题:
(1)写出氯化钠和硫酸铵溶液混合得到硫酸钠晶体的化学方程式: 。
(2)欲制备10.7 g NH4Cl,理论上需NaCl质量为 g。
(3)实验室进行蒸发结晶用到的主要仪器除铁架台、铁圈、酒精灯外,还要有 。
(4)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 。
(5)不用其它试剂,检查NH4Cl产品是否纯净的方法:
操作步骤 | 现象 | 结论 |
取少量氯化铵产品于试管底部, | 表明氯化铵产品纯净 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com