
(10分)(1)下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素 同素异形体 同分异构体 同一种物质 。
①金刚石与“足球烯”C60; ②D与T;

(2)写出下列反应方程式并注明反应类型
① ②
CH2=CH2 → CH3CH2OH → CH3COOCH2CH3
① 反应类型
② 反应类型
科目:高中化学 来源: 题型:
每空2分,共10分)
根据下列五种元素的电离能数据(单位:kJ/mol),回答下面各题。
(1)在周期表中,最可能处于同一族的是( )
A.Q和R B.S和T C.T和U D.R和T E.R和U
(2)电解它们的熔融氯化物或氧化物,阴极电极反应式最可能正确的是( )
A.Q2++2e-→Q B.R2++2e-→R C.S3++3e-→S
D.T3++3e-→T E.U2++2e-→U
(3)它们的氯化物的化学式,最可能正确的是( )
A.QCl2 B.RCl C.SCl3 D.TCl E.UCl4
(4)S元素最可能是( )
A.S区元素 B.稀有气体元素 C.p区元素 D.准金属 E.d区元素
(5)下列元素中,化学性质和物理性质最像Q元素的是( )
A.硼(1s22s22p1) B.铍(1s22s2)C.锂(1s22s1)D.氢(1s1)E 氦(1s2)
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分,每空2分)(1)下列反应中属于氧化还原反应的是 。(填序号)
A. MnO2 + 4HCl(浓)= MnCl2 + Cl2↑+ 2H2O B.SO2+2H2S = 2H2O+3S↓
C.Ba(OH)2 + H2SO4 =BaSO4↓+2H2O D.Cl2+2NaOH= NaCl +NaClO+H2O
(2)已知KMnO4 与浓盐酸发生如下反应:
2KMnO4 + 16HCl(浓)=== 2KCl + 2MnCl2 + 5Cl2↑+8H2O。
在上述反应中,氧化剂是 。用单线桥法标出此反应的电子转移方向和数目。
(3)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
①将这6种物质分别填入下面对应的横线上,组成一个未配平的化学方程式:
________+________+H2SO4→ ________+________+________(填化学式)
②反应中1mol氧化剂得到______mol电子。
查看答案和解析>>
科目:高中化学 来源:2010年湖南省长沙市第一中学高三上学期第四次月考化学卷 题型:填空题
(10分,每空1分)某同学在探究废干电池内的黑色固体回收利用时,进行如图示实验: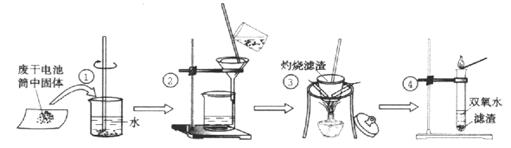
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、三角架 、 ;
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气
体,据此可初步认定黑色固体为 。
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测
滤渣中还存在的物质为 。
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出 其空白处的内容:
其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1、检验Cl— | 取少许滤液于试管中, | | 含有Cl— |
| 2、检验NH4+ | 取少许滤液于试管中, | | 含有NH4+ |
| 3、检验Zn2+ | 取少许滤液于试管中,加入 稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
查看答案和解析>>
科目:高中化学 来源:2015届黑龙江省高一上学期期中考试化学试卷(解析版) 题型:实验题
(8分)下面a~f是中学化学实验中常见的几种仪器:
a.量筒 b.容量瓶 c.托盘天平 d.温度计 e.分液漏斗
(1)标出仪器使用温度的是________(填写编号)。
(2)使用前需要检查是否漏水的是________(填写编号)。
(3)称取10.5 g固体样品(1 g以下使用游码)若样品与砝码错放位置,则实际称取的样品质量为________ g。
(4)配制2 mol·L-1 H2SO4时,用a量取浓H2SO4时视线高于液面,则配得的浓度 (偏高、偏低或无影响)
查看答案和解析>>
科目:高中化学 来源:2010年海南省高二下学期期末考试化学(理)试题 题型:实验题
(10分)某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100 mL稀H2SO4溶液;以0.14 mol·L-1的NaOH溶液滴定上述稀 H2SO425mL,滴定终止时消耗NaOH溶液15mL。
(1)该学生用标准0.14 mol·L-1NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25 mL,注入锥形瓶中,加入指示剂。
B.用待测定的溶液润洗酸式滴定管。 C.用蒸馏水洗干净滴定管。
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
E.检查滴定管是否漏水。 F.另取锥形瓶,再重复操作一次。
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填写): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终点?
。
(2)碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) ,原因是 。
(3)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度为 mol·L-1 (计算出结果到小数点后二位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com