
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
由表中数据可知,随温度升高平衡常数减小,说明升高温度N2(g)+3H2(g)?2NH3(g平衡逆向移动,则正反应为放热反应;
(2)400℃时,2NH3(g)?N2(g)+3H2(g)与N2(g)+3H2(g)?2NH3(g)的平衡常数互为倒数关系;
计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行.
解答 解:(1)N2(g)+3H2(g)?2NH3(g)的平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,由表中数据可知,随温度升高平衡常数减小,说明升高温度N2(g)+3H2(g)?2NH3(g平衡逆向移动,则正反应为放热反应,故a<0,
故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$;小于;
(2)400℃时,2NH3(g)?N2(g)+3H2(g)与N2(g)+3H2(g)?2NH3(g)的平衡常数互为倒数关系,故400℃时,2NH3(g)?N2(g)+3H2(g)的平衡常数为$\frac{1}{0.5}$=2,
此时浓度商Qc=$\frac{\frac{2}{0.5}×(\frac{1}{0.5})^{3}}{(\frac{3}{0.5})^{2}}$=0.89<K=2,反应向正反应进行,v正(N2)>v逆(N2),
故答案为:2;大于;正.
点评 本题考查化学平衡计算,涉及平衡常数及其应用,注意平衡常数只受温度影响,平衡常数及其单位与化学计量数有关.


科目:高中化学 来源: 题型:选择题
| A. | Na2O | B. | Na2O2 | C. | Na2O和Na2O2 | D. | Na2O2和Na |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
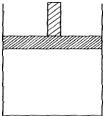 150℃时,向如图所示的容器(密封的隔板可自由滑动,整个过程中保持隔板上部压强不变)中加入4L N2和H2的混合气体,在催化剂作用下充分反应(催化剂体积忽略不计),反应后恢复到原温度.平衡后容器体积变为3.4L,容器内气体对相同条件的氢气的相对密度为5.
150℃时,向如图所示的容器(密封的隔板可自由滑动,整个过程中保持隔板上部压强不变)中加入4L N2和H2的混合气体,在催化剂作用下充分反应(催化剂体积忽略不计),反应后恢复到原温度.平衡后容器体积变为3.4L,容器内气体对相同条件的氢气的相对密度为5.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10s时,再加入一定量的D,平衡向右移动 | |
| B. | 10s时用D物质表示的速率为0.04mol/(L•S) | |
| C. | 10s时,容器中B的浓度为1.6mol•L-1 | |
| D. | 达到平衡时A的转化率为60%,若要在相同条件下反应达到平衡时A的转化率仍为60%,起始加入n(A)=n(B)即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③④ | C. | ①③④ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
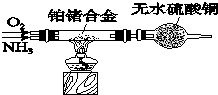 氮及其化合物在很多方面有重要的用途.
氮及其化合物在很多方面有重要的用途.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C(SO42- )为0.02mol/L | B. | 100mL溶液中含有0.01mol Al3+ | ||
| C. | 溶液中一定存在Na+ | D. | 无法确定是否含有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com