


 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源:不详 题型:填空题
| 检测次数 | 溶液中检测出的溶质 |
| 第一次 | KCl K2SO4 Na2CO3 NaCl |
| 第二次 | KCl BaCl2 Na2SO4 K2CO3 |
| 第三次 | Na2SO4 KCl K2CO3 NaCl |
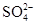 、CO32–和Cl–,该小组进行了如下实验,请你参与探究与分析。
、CO32–和Cl–,该小组进行了如下实验,请你参与探究与分析。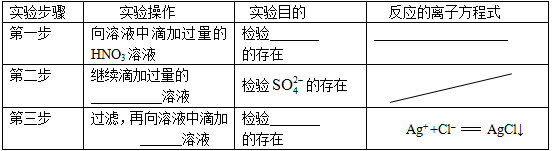
 六种离子。并且甲厂的废水明显呈碱性,因此第二组断定甲厂废水中应含有的三种离子为 、 、 。
六种离子。并且甲厂的废水明显呈碱性,因此第二组断定甲厂废水中应含有的三种离子为 、 、 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| | 错误观点 | 离子方程式 |
| ① | 所有的离子方程式均可以表示一类反应 | |
| ② | 所有酸碱中和反应均可表示为:H++OH-=H2O | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.x=20时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)>c(SO42-) |
| B.x=20时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(Al3+) |
| C.x=60时,溶液中有Ba2+、Al3+、OH-,且c(OH-) = c(Ba2+) |
| D.x=60时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<c(AlO2-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3 | B.FeCl3 | C.CuSO4 | D.Ca(NO3)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5:4 | B.4:5 | C.5:12 | D.12:5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com