
| A. | 再通入少量氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 | |
| B. | 光照一段时间氯水,溶液的pH值增大 | |
| C. | 加入少量固体AgNO3,溶液的pH值减小 | |
| D. | 加入少量水,水的电离平衡向右移动 |
分析 A.氯气与水的反应,加入氯气,溶液为饱和溶液;
B.新制氯水中的次氯酸见光分解生成盐酸;
C.氯离子与银离子反应,溶解平衡向着正向移动,溶液中氢离子浓度最大;
D.氯气与水的反应,加入水,溶液酸性减弱,促进水的电离.
解答 解:在氯水中存在如下平衡:Cl2+H2O?HCl+HClO、H2O?H++OH-、HClO?H++ClO-.
A.氯气溶于水达到平衡后,再通入少量氯气,此时已经为饱和溶液,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$的比值不变,故A错误;
B.新制氯水中的次氯酸见光分解生成盐酸,增大了氢离子浓度,溶液的pH减小,故B错误;
C.加入少量固体AgNO3,银离子与氯离子反应生成AgCl沉淀,氯气的溶解平衡向着正向移动,则溶液中氢离子浓度增大,溶液的pH值减小,故C正确;
D.加入少量的水,相当于增大了水的量,c(H+)下降,对水的电离的抑制作用减弱,水的电离平衡向正反应方向移动,故D正确;
故选CD.
点评 本题考查了化学平衡、电离平衡及其影响,题目难度中等,A选项为易错点,明确电离平衡、化学平衡及其影响因素为解答关键,注意D选项中在水中加酸或碱都抑制了水的电离,酸性或碱性减弱会使水的电离程度增大.


科目:高中化学 来源: 题型:选择题
| A. | CH3COONa | B. | NaHCO3 | C. | NaCl | D. | NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HCl+2Na═2NaCl+H2↑ | |
| B. | 2CH3COOH+Ca(ClO)2═2HClO+Ca(CH3COO)3 | |
| C. | I2+2NaClO3═2NaIO3+Cl2 | |
| D. | 4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A,B,C,D,E是五种短周期元素,A,B,C,D,E分别代表元素符号,他们的原子序数依次增大,A是元素周期表中半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐;D与A同主族,且与E同周期;E元素最外层电子数是其次外层电子数的$\frac{3}{4}$;C与E同主族.请回答下列问题:
A,B,C,D,E是五种短周期元素,A,B,C,D,E分别代表元素符号,他们的原子序数依次增大,A是元素周期表中半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐;D与A同主族,且与E同周期;E元素最外层电子数是其次外层电子数的$\frac{3}{4}$;C与E同主族.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +2价 | B. | +3价 | C. | +4价 | D. | +6价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0~1min,CO的平均反应速率为o.5mol/(L•min) | |
| B. | 增大压强,化学反应速率加快,K增大 | |
| C. | H2S的平衡转化率为71.4% | |
| D. | 平衡后,又加入CO、H2各1mol,平衡逆动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
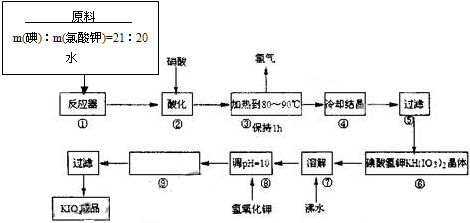
| 温度 | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
查看答案和解析>>
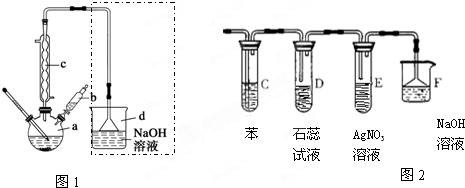
科目:高中化学 来源: 题型:填空题
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com