
分析 化学反应中断开化学键要吸收能量,形成化学键要放出能量,反应物与生成物的总能量大小决定反应热,一般来说,增大浓度、升高温度、加入催化剂等,可增大反应速率,以此解答该题.
解答 解:从能量角度看,断开化学键要吸收热量,一个化学反应是释放能量还是吸收能量取决于反应物和生成物所具有的总能量的相对大小;在化学反应中,浓度越大,化学反应速率越快;温度越低化学反应速率越慢;使用催化剂可以使反应速率加快,
故答案为:吸收; 反应物和生成物所具有的总能量的相对大小; 大; 慢;加快.
点评 本题考查化学反应与能量变化以及反应速率的影响因素,为高频考点,侧重考查学生的分析能力以及双基知识的掌握,难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色退去 | 2min后,出现凝胶 | 酸性:HCl>H2SiO3 |
| B | 在SiO2中加入蒸馏水,振荡 | SiO2溶解 | SiO2是H2SiO3的酸酐 |
| C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁与浓硫酸不反应 |
| D | 向某溶液中先滴加少量氯水,一会儿后滴加KSCN溶液 | 滴加氯水时无明显现象,滴加KSCN溶液后,混合液变成红色 | 原溶液中含有Fe2+,没有Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  实验:振荡后静置,上层溶液颜色保持不变 | |
| B. |  实验:试管溶液中出现气泡,溶液先出现浑浊后变澄清 | |
| C. |  实验:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 | |
| D. | 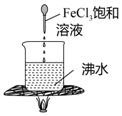 实验:加热至混合液呈红褐色,停止加热,该分散系能产生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现有A、B、C、D、E五种短周期非金属元素,其原子序数依次增大.A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等.C、E是同主族元素,它们的核外均有3个未成对电子.请回答下列问题:
现有A、B、C、D、E五种短周期非金属元素,其原子序数依次增大.A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等.C、E是同主族元素,它们的核外均有3个未成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能发生加聚反应 | B. | 乙烯可以燃烧 | ||
| C. | 苯能使酸性高锰酸钾溶液褪色 | D. | 苯分子中6个碳碳化学键完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3个 | B. | 5个 | C. | 6个 | D. | 7个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;A 分子中能够共平面的原子 最多为8个,写出A与溴的四氯化碳反应的化学方程式
;A 分子中能够共平面的原子 最多为8个,写出A与溴的四氯化碳反应的化学方程式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碘在科研与生活中有重要应用.某兴趣小组用0.50mol•L-1KI、0.2%淀粉溶液、0.20mol•L-1K2S2O8、0.10mol•L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
碘在科研与生活中有重要应用.某兴趣小组用0.50mol•L-1KI、0.2%淀粉溶液、0.20mol•L-1K2S2O8、0.10mol•L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.| 实验序号 | 体积V/mL | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 迄今人类发现的元素中,金属元素和非金属元素种数相近 | |
| B. | 元素周期表有18个纵行16个族,分为主族、副族、第Ⅷ族和零族 | |
| C. | 元素周期表有七个周期,分为短周期和长周期 | |
| D. | 人们在周期表中金属与非金属的分界处可以找到半导体材料,如硅、锗等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com