
| A. | 次氯酸钙有强氧化性,用于饮用水消毒 | |
| B. | 木炭具有还原性,用于制冰箱除味剂 | |
| C. | 氧化铝具有两性,用于工业冶炼铝单质 | |
| D. | 氯化铁溶液呈酸性,用于蚀刻铜电路板 |
分析 A.具有强氧化性可杀菌消毒;
B.木炭具有吸附性;
C.Al为活泼金属,利用电解法冶炼;
D.Cu与氯化铁发生氧化还原反应.
解答 解:A.具有强氧化性可杀菌消毒,则次氯酸钙有强氧化性,用于饮用水消毒,故A正确;
B.木炭具有吸附性,则用于制冰箱除味剂,与其还原性无关,故B错误;
C.Al为活泼金属,利用电解法冶炼,则工业上电解氧化铝冶炼铝单质,与其两性无关,故C错误;
D.Cu与氯化铁发生氧化还原反应,则用于蚀刻铜电路板,与水解显酸性无关,故D错误;
故选A.
点评 本题考查物质的性质及用途,为高频考点,把握物质的性质、发生的反应、性质与用途的关系为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
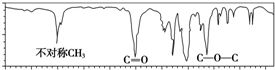
| A. | CH3COOCH2CH3 | B. | CH3CH2COOH | C. | HCOOCH2CH2CH3 | D. | (CH3)2CHCH2COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最外层有1个电子的原子 | B. | 最外层电子排布为ns2的原子 | ||
| C. | 最外层有3个未成对电子的原子 | D. | 次外层无未成对电子的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
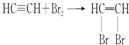
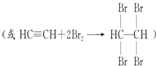 .
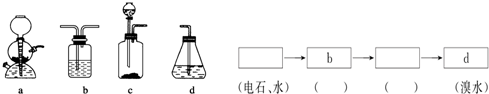
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(SO2):饱和NaHCO3溶液 | B. | NO(NO2):水 | ||
| C. | Cl2(HCl):NaOH溶液 | D. | Na2CO3固体(NaHCO3):加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
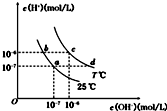
| A. | a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42- | |
| B. | b点对应的溶液中大量存在:ClO-、Ba2+、OH-、I- | |
| C. | c点对应的溶液中大量存在:Na+、Ba2+、Cl- HCO3- | |
| D. | d点对应的溶液中大量存在:Na+、K+、SO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
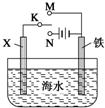 对金属制品进行抗腐蚀处理,可延长其使用寿命.
对金属制品进行抗腐蚀处理,可延长其使用寿命.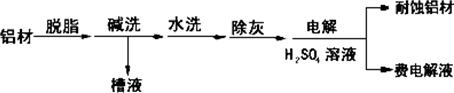
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com