
【题目】氯碱工厂生产的氯气和氢气可以进一步用于生产盐酸,主要过程如下:

(1)其中关键的一步为氯气和氢气在燃烧管口燃烧生成HCl,氯气有毒,应采取的措施是____。合成盐酸厂要求合成气中的HCl的含量要大于97%,试用最简便的方法进行分析是否含量大于97%____。
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,反应的化学方程式为__。
(3)某同学欲证明盐酸与氯化氢气体性质不同,他分别向A、B、C三支洁净试管中各放入一片干燥的蓝色石蕊试纸,然后往A试管内加入盐酸,试纸显___色,往B试管中通入干燥的氯化氢气体,试纸显___色.最后向C试管中加入物质___(填化学式),他之所以加入这种物质的理由是____。
【答案】先通氢气点燃,再通Cl2 用100mL刻度瓶收集满HCl气体,置于水中,水升至97mL以上即认为符合要求 Cl2+2NaOH=NaCl+NaClO+H2O 红色 蓝色 H2O 证明单独的氯化氢气体或水均不能使蓝色石蕊试纸变色
【解析】
(1)氯气有毒,为保证氯气完全反应,氢气应过量,则应从外管通入氢气,从内管通入氯气,故答案为:先通氢气点燃,再通Cl2;
合成盐酸厂要求合成气中的HCl的含量要大于97%,用100mL刻度瓶收集满HCl气体,置于水中,水升至97mL以上即认为符合要求;
(2)氯碱工厂生产的氯气和氢氧化钠溶液可以用于制取“84消毒液”,氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O;
(3)盐酸是一种酸,盐酸溶液中的氢离子能使蓝色石蕊试液变成红色,氯化氢既不属于酸也不属于碱,不能能使蓝色石蕊试纸变色,仍为蓝色;
盐酸能使蓝色石蕊试纸变红,盐酸是氯化氢气体的水溶液,氯化氢气体和水能不能使蓝色石蕊试纸变红呢?通过B试管中实验已经排除了单独的氯化氢气体不能使蓝色石蕊试纸变色,还需要进一步排除单独的水也不能使使蓝色石蕊试纸变色,要利用控制变量法向C试管中单独加入水进行试验,水的化学式为H2O。
故答为:红色;蓝色;H2O;证明单独的氯化氢气体或水均不能使蓝色石蕊试纸变色。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如图装置进行有关实验。请回答:
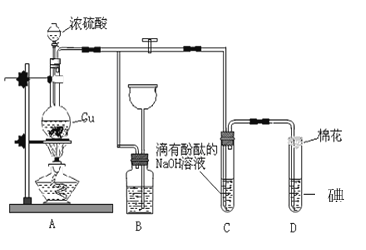
(1)装置A中发生的化学反应的化学方程式: _________________________________。
(2)装置B 的作用是__________________,B中广口瓶内应盛放的液体是_________(填序号)
①水 ②澄清石灰水
③Na2CO3溶液 ④饱和的NaHSO3 溶液
(3)装置C和D 中产生的现象相同,但原因却不同。C中反应的方程式:_______________________________________,而D 中则是由于SO2 具有_______性,D中反应的方程式:________________________。
(4)实验中,0.1molCu与含0.2mol硫酸的溶液反应后,铜和硫酸都有剩余。 可以证明有余酸的实验方案是___________
A.可再加入锌粒 B.可再加入氯化钡溶液
C.再加入银粉 D.再滴入碳酸氢钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为某化学反应速率一时间图。在t1时刻升高温度或增大压强,都符合图所示变化的反应是

A. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)ΔH<0
4NO(g)+6H2O(g)ΔH<0
B. 2SO2(g)+O2(g)![]() 2SO3(g)ΔH< 0
2SO3(g)ΔH< 0
C. H2(g)+I2(g)![]() 2HI(g)ΔH>0
2HI(g)ΔH>0
D. C(s)+H2O(g)![]() CO(g)+H2(g)ΔH>0
CO(g)+H2(g)ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知地球上元素原子各电子层最多能容纳的电子数为2n2(n表示电子层序数),若X星球上的元素原子各电子层最多能容纳的电子数为n(n+1),n表示电子层数,该星球上元素原子的电子排布的其他规则与地球相同,回答下列问题:
(1)X星球上的质子数为5的元素原子最外层电子数为___个;
(2)X星球上的质子数为9的元素原子的结构示意图为___,该元素属于___元素(填“金属”或“非金属”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在一个密闭容器中进行如下反应:NO(g)+CO(g) ![]()
![]() N2(g)+CO2(g) ΔH=-373.2 kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2 kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A. 加催化剂同时升高温度 B. 加催化剂同时增大压强
C. 升高温度同时充入N2 D. 降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温、催化剂条件下,某反应达到平衡,平衡常数K=c(CO)·c(H2O)/c(CO2)·c(H2)恒容时,温度升高,H2浓度减小.下列说法正确的是
A. 该反应的焓变为负值
B. 升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
C. 2CO2(g)+2H2(g)2CO(g)+2H2O(g) 的平衡常数K1=K2
D. 若恒容、恒温下充入CO,则K值变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:

依据上图,完成下列填空:
(1)在电解过程中,所发生的反应方程式为______________________________________。与电源_______极相连的电极附近溶液滴入酚酞显红色。阳极产物是______________,实验室用__________________________检验该物质。
(2)如果粗盐中SO42含量较高,必须添加钡试剂除去SO42,该试剂可以是_____________________。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2 d.BaCO3
(3)为有效除去Ca2+、Mg2+、SO42,加入试剂的合理顺序为__________________。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A. 原子半径:W>Z>Y>X>M
B. 常见气态氢化物的稳定性:X<Y<Z
C. 1 mol WM溶于足量水中完全反应,共转移2 mol电子
D. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述,不正确的是( )
A. 新制的氯水中,溶质既有分子又有离子
B. 新制的氯水是无色透明的液体,有酸性和漂白性
C. 光照氯水有气泡逸出,该气体是O2
D. 氯水放置数天后酸性将增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com