
【题目】下列图示与对应的叙述相符合的是
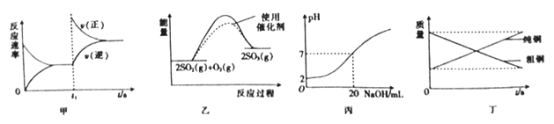
A.图甲表示t1时刻增加反应物浓度后v(正)和v(逆)随时间的变化
B.图乙表示反应2SO2(g)+O2(g)=2SO3(g) △H<0 在两种条件下物质能量随反应过程的变化
C.图丙表示25℃时用0.01mol/LNaOH溶液滴定20.00 mL 0.01mol/LHCl溶液时pH随NaOH 溶液体积的变化
D.图丁表示电解精炼铜时纯铜和粗铜的质量随时间的变化
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关离子晶体的数据大小比较不正确的是
A. 熔点:NaF>MgF2>AlF3B. 晶格能:NaF>NaCl>NaBr
C. 阴离子的配位数:CsCl>NaClD. 硬度:MgO>CaO>BaO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图装置制取某些气体并进行一系列的性质探究。
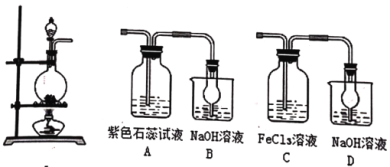
请回答:
(1)下列说法正确的是_____。
A.实验开始时,打开装置Ⅰ中分液漏斗的旋塞,液体能顺利滴下
B.将装置Ⅰ与Ⅱ连接,制取Cl2并检验其性质,其中B装置的作用为防倒吸
C.过量的铜与浓硫酸在装置Ⅰ中反应,反应后的溶液中溶质仅为硫酸铜
D.将装置Ⅰ和Ⅱ连接,制取SO2并检验其性质,A中的紫色石蕊试液只能变红
(2)将装置Ⅰ和装置Ⅲ连接,制取SO2并检验其性质。C中溶液颜色由棕黄色逐渐变浅绿色,反应的离子方程式为:_____,反应结束后C中的阴离子的检测方法为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置,下图为电池示意图,下列有关氢氧燃料电池的说法正确的是:

A. 该电池工作时电能转化成化学能
B. 该电池中a是正极
C. 外电路中的电子由电极b通过导线流向a
D. 该电池的总反应为:2H2+O2==2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1
C. -330kJ·mol-1 D. +330kJ·mlo-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.16g·L-1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
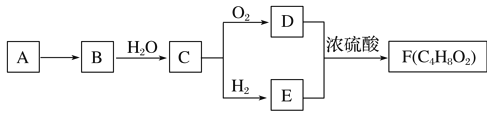
请回答:
(1)有机物D中含有的官能团名称是___。
(2)D+E→F的反应类型是___。
(3)有机物A在高温下转化为B的化学方程式是___。
(4)下列说法正确的是___。
(A)有机物E与金属钠反应比水与金属钠反应要剧烈
(B)有机物D、E、F可用饱和Na2CO3溶液鉴别
(C)实验室制备F时,浓硫酸主要起氧化作用
(D)有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。
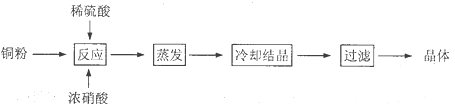
根据题意完成下列填空:
(1)理论上,为了制得纯净的CuSO4·5H2O晶体,需要消耗稀硫酸、稀硝酸溶质物质的量之比为___。
(2)实际生产过程中对所加稀硝酸的浓度控制要求比较高,通常用标准氢氧化钠溶液来滴定。滴定过程中若用酚酞作指示剂,终点现象是___。
(3)请在图中画出滴定过程中溶液的pH随所滴加氢氧化钠溶液体积的变化的曲线图(要求过A点)。____
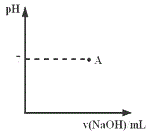
(4)上述使用的标准氢氧化钠溶液已经通过基准物质的标定。下列物质中通常可用来标定碱液的基准物质是___。
A.醋酸 B.草酸 C.苯甲酸 D.苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为![]() 。
。
阳离子 |
|
阴离子 |
|
甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在无色火焰上灼烧,未出现黄色火焰
②取少量溶液,加入![]() 溶液无明显变化。
溶液无明显变化。
③另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
④向③中所得的溶液中加入![]() 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
(1)步骤①使用的焰色反应属于___(填“物理”或“化学”)变化
(2)③中加入少量盐酸生成无色气体的离子方程式是____
(3)该溶液中一定含有的阳离子有___,一定含有的阴离子有___
(4)检验溶液中存在![]() 的方法是_____
的方法是_____
(5)取![]() 该溶液,向溶液中加入过量的稀氢氧化钠溶液,充分反应后,过滤、洗涤,将沉淀在空气中灼烧后得到的固体质量为___g
该溶液,向溶液中加入过量的稀氢氧化钠溶液,充分反应后,过滤、洗涤,将沉淀在空气中灼烧后得到的固体质量为___g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下列装置可以制备无水氯化铁。下列有关说法正确的是( )
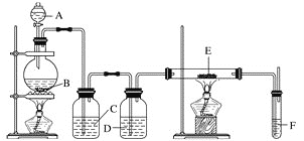
A. 烧瓶B中制备氯气的反应物为MnO2和稀盐酸
B. 装置C、D中分别盛有浓硫酸、饱和食盐水
C. 装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁
D. 装置F的目的是检验有无氯气逸出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com