
���� ��1������Ԫ�ػ��ϼ����ߵķ�Ӧ��Ϊ��ԭ��������������Ӧ�õ������������Ԫ�ػ��ϼ۽��͵ķ�Ӧ��Ϊ��������������ԭ��Ӧ�õ���ԭ���
FeS2����FeԪ�ػ��ϼ۲��䣬SԪ�ػ��ϼ���-1������Ϊ���ᡢ���������е�+6�ۣ�
��2��Zn�����ᷴӦ��������п������������Hԭ���غ������Ҫ�������ʵ�����
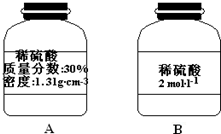
��3��û��240mL����ƿ��Ӧѡ��250mL����ƿ������n=cV������������ʵ���������c=$\frac{1000�Ѧ�}{M}$����30%ϡ��������ʵ���Ũ�ȣ��ٸ���V=$\frac{n}{c}$������Ҫ30%����������
������������Һ������������ʵ���Ӱ�죬�ٸ���c=$\frac{n}{V}$�ж϶�������ҺŨ��Ӱ�죮
��� �⣺��1��FeS2����FeԪ�ػ��ϼ۲��䣬SԪ�ػ��ϼ���-1������Ϊ���ᡢ���������е�+6�ۣ�FeS2�ǻ�ԭ��������������FeSO4��H2SO4������1mol FeS2��ȫ��Ӧʱ��ת�Ƶĵ���Ϊ1mol��2��[6-��-1��]=14mol��
�ʴ�Ϊ����ԭ��FeSO4��H2SO4��14��
��2��Zn�����ᷴӦ��������п����������������Ϊ$\frac{0.224L}{22.4L/mol}$=0.01mol������Hԭ���غ㣺n��H2SO4��=n��H2��=0.01mol��
�ʴ�Ϊ��0.01��
��3��û��240mL����ƿ��Ӧѡ��250mL����ƿ����Ҫ��������ʵ���Ϊ0.25L��2mol/L=0.5mol������c=$\frac{1000�Ѧ�}{M}$��֪��30%ϡ��������ʵ���Ũ��Ϊ$\frac{1000��1.31��30%}{98}$mol/L��4mol/L������Ҫ30%��������Ϊ$\frac{0.5mol}{4mol/L}$=0.125L=125.0mL��
��ϡ�͵�����ת�Ƶ�����ƿ�к�δϴ���ձ�����������ƿ��������������ʵ���ƫС��������ҺŨ��ƫ�ͣ��ʷ��ϣ�
�ڳ��Ƚ���Һע������ƿ�в����ݣ���ȴ����Һ���ƫС��������ҺŨ��ƫ�ߣ��ʲ����ϣ�
��ҡ�Ⱥ���Һ����ڿ̶��ߣ�������Һ������ƿ����ƿ��֮�䣬�ټ�ˮ����Һ���ƫ��������ҺŨ��ƫ�ͣ��ʷ��ϣ�
����Ҫ��ˮ���ж��ݣ�����ƿ��ԭ����������ˮ����Ӱ����ҺŨ�ȣ��ʲ����ϣ�
�ʴ�Ϊ��250mL����ƿ��125.0mL���٢ۣ�
���� ���⿼��������ԭ��Ӧ��һ�����ʵ���Ũ����Һ���ƣ�����ƴ������Ŀ��ע����ݻ��ϼ�����������ԭ��Ӧ�����������c=$\frac{n}{V}$������Һ����ԭ������������


 ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
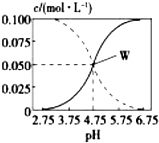 25��ʱ���ɴ���ʹ����ư�һ����������γɵ���Һʼ�ձ���c��CH3COOH��+c��CH3COO-��=0.1mol/L������Һ��c��CH3COOH����c��CH3COO-����pH�Ĺ�ϵ��ͼ��ʾ�������йظ���Һ����������ȷ���ǣ�������
25��ʱ���ɴ���ʹ����ư�һ����������γɵ���Һʼ�ձ���c��CH3COOH��+c��CH3COO-��=0.1mol/L������Һ��c��CH3COOH����c��CH3COO-����pH�Ĺ�ϵ��ͼ��ʾ�������йظ���Һ����������ȷ���ǣ�������| A�� | pH=5����Һ�У�c��CH3COOH����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | W������ʾ����Һ�У�c��Na+��=c��CH3COOH�� | |
| C�� | pH=3����Һ�У�c��H+��+c��Na+��+c��CH3COOH��=0.1mol/L | |
| D�� | ��ͼ�����ø��¶���CH3COOH�ĵ��볣��Ka=10-4.75 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al2O3$��_{��}^{NaOH��aq��}$NaAlO2��aq��$\stackrel{CO_{2}}{��}$Al��OH��3 | |
| B�� | S$��_{��ȼ}^{O_{2}}$SO3$\stackrel{H_{2}O}{��}$H2SO4 | |
| C�� | Mg��OH��2$\stackrel{����}{��}$MgCl2��aq��$\stackrel{����}{��}$��ˮMgCl2 | |
| D�� | Fe$��_{����}^{H_{2}O}$Fe2O3$\stackrel{����}{��}$FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʽΪC4H10�������Ķ���ȡ���� | |
| B�� | ����ʽΪC4H10O2���л��� | |
| C�� | �ұ���һ��ȡ���� | |
| D�� | ��H2�ӳ�����2-������ĵ�ϩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


| H2C204 | Ka1=5.36��10-2 | Ka2=5.35��10-5 |
| HF | Ka=6.32��10-4 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȷ�Χ/�� | 120-220 | 300-350 | 450-500 | ����600 |
| ����/g | 22.05 | 11.25 | 11.85 | 13.05 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | .�����ᱵ����ϡ�����У�BaSO3+2H+�TBa2++SO2��+H2O | |
| B�� | ���������Һ�м�������������Һ��Ba2++SO42-�TBaSO4�� | |
| C�� | ��ˮ������ͨ������CO2��SiO32-+2CO2+3H2O�TH4SiO4��+2HCO3- | |
| D�� | ��NaOH��Һ���շ����еĵ������NO+NO2+2OH-�T2NO2-+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ����������뷴Ӧ�������֮���Ϊ��Ӧ�ʱ� | |
| B�� | ��Ӧ���������С�ڷ�Ӧ������ʣ��÷�ӦΪ���ȷ�Ӧ | |
| C�� | ͬһ��Ӧ�ڲ�ͬ�¶��½��У����ʱ�����ͬ�� | |
| D�� | ��֪2NO2��g���TN2O4��g����H1��N2O4��g���T2NO2��g����H2�����H1=-��H2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com