
下列浓度关系正确的是( )
A.氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)]
B. 氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-)
D.Na2CO3溶液中:c(Na+)>c(CO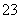 )>c(OH-)>c(HCO
)>c(OH-)>c(HCO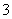 )>c(H+)
)>c(H+)
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)。下列关于元素R的判断中一定正确的是 ( )。
| I1 | I2 | I3 | I4 | …… | |
| R | 740 | 1 500 | 7 700 | 10 500 |
①R的最高正价为+3价 ②R元素位于元素周期表中第ⅡA族 ③R元素第一电离能大于同周期相邻元素 ④R元素基态原子的电子排布式为1s22s2
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
把图2中的物质补充到图1中,可得到一个完整的氧化还原型离子方程式(未配平):
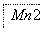 ……
……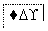
图1
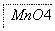
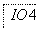
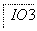
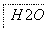

图2
对于该离子方程式的说法不正确的是 ( )。
A.IO 作氧化剂
作氧化剂
B.氧化性:Mn2+>IO
C.氧化剂与还原剂的物质的量之比为5∶2
D.若有2 mol Mn2+参加反应时,则转移10 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型消毒剂,工业上制备高铁酸钠有下列四种方法:
a.2Fe(OH)3+3NaClO+4NaOH===2Na2FeO4+3NaCl+5H2O;
b.2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑;
c.Fe2O3+3Na2O2===2Na2FeO4+Na2O;
d.Fe(NO3)3+NaOH+Cl2―→Na2FeO4+NaNO3+NaCl+H2O。
请回答下列问题:
(1)下列判断正确的是________(填序号)。
A.方法a、b、c都可在水溶液中进行
B.根据a、b可知NaClO、Na2O2的氧化性均强于Na2FeO4的
C.FeSO4只有还原性,没有氧化性
D.能用KSCN溶液检验b的产物中是否含有FeSO4
(2)对于方法c下列说法正确的是________(填序号)。
A.Na2O2既是氧化剂又是还原剂
B.还原产物只有Na2O
C.3 mol Na2O2发生反应,有6 mol电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
(3)对于方法d,请回答下列问题:
①氧化剂与还原剂的物质的量之比为________。
②写出Na2FeO4与H2O反应的离子方程式:____________________________,
请你推测Na2FeO4除了能消毒杀菌外,另一个用途是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
今有下列四种酸溶液:(A)c(H+)=0.1 mol·L-1的盐酸,(B)c(H+)=0.1 mol·L-1的硫酸,(C)c(H+)=0.1 mol·L-1的醋酸,(D)0.01 mol·L-1的醋酸。
(1)四种酸中,c(H+)的大小关系是(用标号表示,下同)______________。
(2)四种溶液的溶质的物质的量浓度的大小关系是______。
(3)取等体积的四种溶液分别无限稀释,酸分子可电离生成的全部H+的物质的量的大小关系是__________________。
(4)取等体积的四种溶液,分别加入等量锌粉,刚开始反应时反应速率的大小关系是________________________________________________________________________;
当反应结束后,发现有一种酸有剩余,则此酸为__________。
(5)取等体积的四种溶液分别加入NaOH溶液,当完全中和时,消耗NaOH的物质的量的关系是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.1 mol C7H16中含有23 mol共价键
B.标准状况下,1.12 L NH3中含有0.5 mol e-
C.常温常压下,22 g CO2中所含分子数是0.5 mol
D.40 g NaOH溶于1 L水,所得溶液中c(Na+)=1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关颜色变化错误的是( )
A.在4mL0.1mol/L的K2Cr2O7溶液中滴加数滴1mol/LNaOH溶液,溶液颜色从橙色变成黄色
B.在试管中加入少量氯化钴晶体,滴加浓盐酸溶解后加水稀释至紫色,将试管置于热水中片刻,溶液颜色变成粉红色
C.向血红色的Fe(SCN)3溶液中加入少量KI固体,溶液颜色变浅
D.用50mL针筒抽取30mL红棕色的NO2气体并封住注射孔,当用力推压活塞,压缩针筒中的气体(此过程中不考虑温度变化),从针筒顶端观察,气体颜色逐渐变浅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com