
| A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、小苏打与醋酸反应:HCO3-+H+═CO2↑+H2O |
| C、金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-?+H2↑ |
| D、氯化铝溶液与过量氨水反应:3NH3?H2O+Al3+=Al(OH)3↓+3NH4+ |


科目:高中化学 来源: 题型:

| SOCI2 |
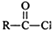
 +
+ →
→ +HCI
+HCI 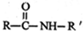
| NaOH溶液 |

查看答案和解析>>
科目:高中化学 来源: 题型:
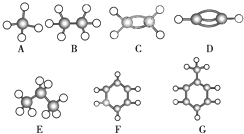 A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
A~G是几种烃的分子球棍模型(如图),据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液:Al3+、K+、Cl-、S2- |
| B、滴加酚酞显红色的溶液:Na+、ClO-、NO3-、Cl- |
| C、滴加甲基橙显红色的溶液:Fe2+、NH4+、SO42-、NO3- |
| D、c(H+)=c(OH-)的溶液:Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、是氧化还原反应,Na2O2是氧化剂,CO2是还原剂 |
| B、是氧化还原反应,CO2是氧化剂,Na2O2是还原剂 |
| C、不是氧化还原反应,是碱性氧化和酸性氧化物反应 |
| D、是氧化还原反应,Na2O2既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
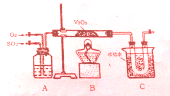 某研究性学习小组为在实验室再现二氧化硫催化氧化的过程,应制取少量二氧化硫晶体,设计了如下图所示装置,已知三氧化硫通水生成硫酸并放出大量热,容易形成酸液,试回答:
某研究性学习小组为在实验室再现二氧化硫催化氧化的过程,应制取少量二氧化硫晶体,设计了如下图所示装置,已知三氧化硫通水生成硫酸并放出大量热,容易形成酸液,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | L层上有2对未成对电子 |
| X | 最外层电子数是次外层电子数的3倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
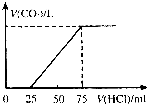 有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液.向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡,使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如图所示.
有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液.向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡,使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、没有洗涤烧杯和玻璃棒 |
| B、定容时凹液面最低点低于刻度线 |
| C、容量瓶用蒸馏水洗涤干净后没有进行干燥就移入所配制溶液 |
| D、转移过程中有少量溶液溅出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com