
| A. | 反应热就是反应中放出的能量 | |
| B. | 在101 kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 | |
| C. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少 | |
| D. | 由C(石墨)═C(金刚石)△H=+1.9 kJ•mol-1可知,石墨稳定 |
分析 A.反应热是指反应过程中所放出或吸收的热;
B.在一定条件下,单位质量的物质完全燃烧时的热效应叫做该物质的热值;
C.硫蒸汽比硫固体所含能量高;
D.物质的能量越低越稳定.
解答 解:A.应热是化学反应过程中吸收或放出的热量,故A错误;
B.在一定条件下,单位质量的物质完全燃烧时的热效应叫做该物质的热值,C燃烧必须是生成CO2时放出的热量才是C的热值,选项未指明碳完全燃烧生成二氧化碳,故B错误;
C.因为硫固体变为硫蒸气要吸热,所以等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多,故C错误;
D.比较稳定性应比较其能量的高低,由C(石墨)-→C(金刚石)△H=+1.9 kJ•mol-1可知,金刚石能量高,不稳定,故D正确;
故选D.
点评 本题考查了反应热的定义、分类和意义,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意燃烧热的定义中要求生成稳定的氧化物.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
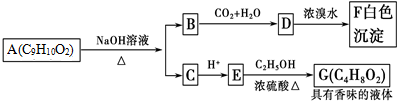
| A. | 根据图示可推知D为苯酚 | |
| B. | G的同分异构体中属于酯且能发生银镜反应的只有两种 | |
| C. | 上述各物质中能发生水解反应的有A、B、D、G | |
| D. | A的结构中含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:X>Y>Z | B. | 原子序数:X<Y<Z | ||
| C. | 气态氢化物稳定性:X<Y<Z | D. | 非金属性:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解的主要目的是提高汽油等轻质油的产量与质量,石油催化裂化的主要目的是得到更多的乙烯、丙烯等气态短链烃 | |
| B. | 分子式为C3H7C1的有机物有三种同分异构体 | |
| C. | 甲烷、苯、乙醇、乙酸和乙酸乙酯在一定条件下都能发生取代反应 | |
| D. | 向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素Q所形成的氧化物只有一种 | |
| B. | 元素M的最高价氧化物对应的水化物为强酸 | |
| C. | 元素C、D、N的最高价氧化物对应的水化物两两之间可发生反应 | |
| D. | 氢化物的稳定性:Q>M |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 试剂B | 湿润的试纸A | 结论 |
| A | 碘水 | 淀粉试纸变蓝 | 碘具有氧化性 |
| B | 浓氨水、生石灰 | 蓝色石蕊试纸变红 | 氨气为碱性气体 |
| C | Na2SO3、硫酸 | 品红试纸褪色 | SO2具有漂白性 |
| D | Cu、浓硝酸 | 淀粉KI试纸变蓝 | NO2为酸性气体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
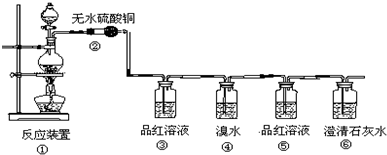
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com