
【题目】下列叙述不正确的是
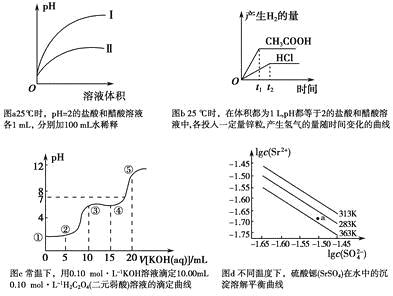
A.图a中,曲线Ⅱ表示醋酸溶液加100 mL水稀释的图像
B.图b中,可能各投入的锌粒颗粒大小相同且质量均为0.65 g
C.图c中,在①、②、③、④、⑤各点的溶液中所含阴离子种类不同
D.图d中,三个不同温度中,313 K时Ksp(SrSO4)最大;且283 K时,图中a点对应的溶液是不饱和溶液
【答案】C
【解析】
A.盐酸是强酸,完全电离,醋酸是弱酸,部分电离,相同温度下,相同pH值的盐酸和醋酸溶液,醋酸浓度大,溶液稀释时,醋酸进一步电离,其溶液中pH小于盐酸的pH,故Ⅱ应为醋酸稀释时的pH值变化曲线,故A正确;
B.1L、pH值等于2的盐酸溶液中c(H+)=0.01mol/L,n(H+)=0.01mol,1L、pH值等于2的醋酸溶液中存在电离平衡,平衡状态下氢离子浓度c(H+)=0.01mol/L,n(H+)=0.01mol,但溶液中醋酸的物质的量大于0.01mol;0.65g锌粒物质的量=![]() =0.01mol,锌和酸反应Zn+2H+=Zn2++H2↑,盐酸酸溶液中氢离子不足,锌剩余0.005mol,醋酸溶液中存在电离平衡,平衡状态下的氢离子不足,但随着反应进行,醋酸又电离出氢离子进行反应,放出的氢气一定比盐酸多,开始时由于氢离子浓度相同,开始的反应速率相同,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以反应速率快,故B正确;
=0.01mol,锌和酸反应Zn+2H+=Zn2++H2↑,盐酸酸溶液中氢离子不足,锌剩余0.005mol,醋酸溶液中存在电离平衡,平衡状态下的氢离子不足,但随着反应进行,醋酸又电离出氢离子进行反应,放出的氢气一定比盐酸多,开始时由于氢离子浓度相同,开始的反应速率相同,反应过程中醋酸溶液中的氢离子浓度始终比盐酸溶液中的氢离子浓度大,所以反应速率快,故B正确;
C.无论反应怎样,在①、②、③、④、⑤各点的溶液中都含有阴离子包括草酸根离子、草酸氢根离子、还有氢氧根离子,所以阴离子种类相同,故C错误;
D.由图象可知:在相同条件下,温度越低,c(SO42-)c(Sr2+)越大,Ksp(SrSO4)越大,a点在283K的下方,属于不饱和溶液,故D正确;
故选:C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在最新的家用汽车的调查中发现,新车中气体的质量不符合标准。汽车污染主要来源于汽车配件及材料,它们都会产生大量的有毒有机物。其中一种有毒物质为A,为了测定有机物A的结构,做如下实验:
①将9.2g该有机物完全燃烧,生成标况下15.68L的CO2和7.2g水;
②用质谱仪测定其相对分子质量,得如图一所示的质谱图;

(1)则由图可知该分子的相对分子质量是___,有机物A的分子式为____。
(2)用核磁共振仪处理该化合物得到四个峰,且面积之比是1∶2∶2:3,则有机物的名称为___,其苯环上的一氯代物有___种。若将有机物A与氢气完全加成,则加成后的有机物的一氯代物共有___种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,![]() 的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是
的这四种溶液pH与该元素原子半径的关系如图所示。下列说法正确的是![]()

A.简单离子半径:![]()
B.Y与W形成的化合物分子可能是非极性分子
C.基态原子的第一电离能:![]()
D.X和Y的最高价氧化物对应的水化物恰好中和时,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向体积恒定的密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
A.容器内压强不随时间变化
B.v正(X)=2v逆(Y)
C.容器内X、Y、Z的浓度之比为1︰2︰2
D.单位时间消耗0.1mol X同时生成0.2mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH<0、ΔS>0
B.加热Na2CO3溶液,![]() 增大
增大
C.由热化学方程式2CO(g)+O2(g)=2CO2 (g)ΔH=-566 kJ·mol-1可知,CO的燃烧热是566 kJ·mol-1
D.中和等体积、等浓度的醋酸和盐酸,醋酸消耗的NaOH的物质的量小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:图甲是由某温度下![]() 、
、![]() 分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL
分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化图.图乙是常温下向100mL![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
溶液,混合溶液的pH变化图.如图所示与推测的结论相符的是
图甲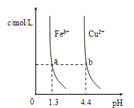 图乙
图乙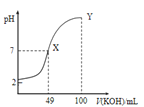
A.由图甲知:![]()
B.由图甲知:a、b点溶液中![]() ,b点的大
,b点的大
C.由图乙知:HA为强酸
D.由图乙知:Y点对应的溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
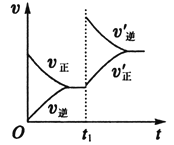
【题目】在一定体积的密闭容器内发生某气体体系反应,根据如图填空。
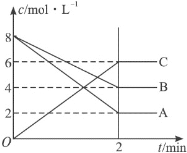
(1)反应物是___,生成物是____。
(2)在2min内A的平均反应速率为___mol·L-1·min-1。
(3)该反应的化学方程式是__![]() ___。
___。
(4)写出此反应的平衡常数表达式___(用物质A、B、C表示),增大压强,平衡向___(填“正”或“逆”)反应方向移动,K___(填“增大”、“减小”或“不变”)。
(5)转化率为已反应的物质的量与初始物质的量比值,B的转化率为___,若升高温度,B的转化率增加,则正反应是___(填“吸热”或“放热”)。
(6)2分钟后的某时刻(t1)改变某一条件使平衡移动,符合如图所示的条件是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4- 、Fe(SCN)3 等。
(1)基态铁原子核外电子排布式为________________.
(2)科学研究表明用 TiO2 作光催化剂可将废水中 CN- 转化为OCN-,并最终氧化为 N2 、CO2。OCN- 中三种元素的第一电离能由大到小的顺序为_________。
(3)与 CN- 互为等电子体的一种分子为________________(填化学式);1mol Fe(CN)63- 中含有![]() 键的数目为________________。
键的数目为________________。
(4)铁的另一种配合物Fe(CO)5 熔点为 —20.5℃,沸点为 103℃,易溶于CCl4,据此可以判断Fe(CO)5 晶体属于________________(填晶体类型)。
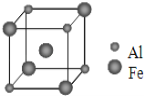
(5)铁铝合金的一种晶体属于体心立方结构,其晶胞可看成由 8 个小体心立方结构堆砌而成。已知小立方体如图所示,该合金的化学式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2CO3 溶液存在水解平衡:CO32-+H2O![]() HCO3-+OH-。下列说法正确的是()
HCO3-+OH-。下列说法正确的是()
A.加入 NaOH 固体,溶液 pH 减小
B.稀释溶液,水解平衡常数增大
C.升高温度,![]() 减小
减小
D.加入 CaCl2 固体,平衡向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com