
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,5.6 L O2作氧化剂时转移电子数一定为NA
B.用惰性电极电解CuSO4溶液后,如果加入0.1 mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA
C.已知3BrF3+5H2O=HBrO3+Br2+9HF+O2↑ 如果有5 mol H2O参加氧化还原反应,则由水还原的BrF3分子数目为3NA
D.142 g Na2SO4和Na2HPO4固体混合物中,阴阳离子总数为3NA
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源:2016届吉林省高三上第四次摸底考试化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值。下列说法不正确的是
A.28 g由C2H4和C3H6组成的混合物中含有氢原子的数目为4 NA
B.1 L 0.1 mol·L-1的NH4Cl溶液中含有Cl-数目为0.1NA
C.1 mol Na2O2固体与足量CO2反应转移电子数为1NA
D.标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省雅安市高一上学期12月月考化学试卷(解析版) 题型:实验题
小明很喜欢化学实验课,今天要学习“探究铁及其化合物的氧化性或还原性”。
(1)实验前小明预测说:Fe2+肯定既有还原性又有氧化性。你认为他预测的依据是: 。
(2)小明欲用实验证明他的预测。实验室提供了下列试剂:3%的H2O2溶液、锌粒、铜片、0.1mol·L-1FeCl2溶液、KSCN溶液、新制氯水。
①若小明计划在0.1mol·L-1FeCl2溶液滴入新制氯水,探究Fe2+的还原性,你预计可能发生的反应和现象是: ________ (写离子方程式)、溶液由浅绿色变 色。
②实验中,小明发现现象不太明显,老师分析可能是产物的含量太低,建议可以通过检验Fe2+被氧化的产物Fe3+的存在以获取证据。你认为可选 滴入小明所得的混合液中,并通过溶液出现 色的现象,证明小明的观点和实验方案都是正确的。
③对于证明Fe2+具有氧化性,小明认为金属单质都具有还原性,并分别将铜片、锌粒投入FeCl2溶液中,结果铜片没变化,锌粒逐渐变小。由此说明三种金属的还原性由强至弱的顺序为: 。
(3)小明分析H2O2中氧元素显-1价(中间价),并提出疑问:H2O2与FeCl2的反应时,Fe2+还作氧化剂吗?
①请你为小明梳理相关问题:若Fe2+在反应中表现出氧化性应转化成 (填微粒符号,下同),若Fe2+在反应中表现出还原性应转化成 。
②实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质。除杂的方法是: ,相关反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上12月月考化学试卷(解析版) 题型:选择题
已知某温度下CH3COOH和NH3•H2O 的电离常数相等,现向10mL浓度为0.1mol•L?1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中下列说法正确的是
A.水的电离程度始终增大
B.当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO?)
C.c(CH3COOH)与c(CH3COO?)之和始终保持不变
D.c(NH4+)/c(NH3•H2O)先增大再减小
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期期末理综化学试卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.常温下,0.1 mol/L Na2S溶液中存在:c(OH-) = c(H+) + c(HS-) + c(H2S)
B.常温下,pH为1的0.1 mol/L HA溶液与0.1 mol/L NaOH溶液恰好完全反应时,溶液中一定存在: c (Na+) = c(A-) > c(OH-) = c(H+)
C.常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)=0.1 mol/L:
c(Na+) = c(CH3COOH) > c(CH3COO-) > c(H+) = c(OH-)
D.常温下,将0.1 mol/L CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中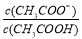 的值减小到原来的
的值减小到原来的
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期12月月考化学试卷(解析版) 题型:选择题
现代家居装修材料中,普遍存在着甲醛、苯及苯的同系物等有毒物质,如果不注意处理就会对人体产生极大的危害。按照有机物的分类,甲醛属于醛。下列各项对有机物的分类方法与此方法相同的是( )
① 属于环状化合物;②
属于环状化合物;②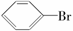 属于卤代烃;
属于卤代烃;
③ 属于链状化合物;④
属于链状化合物;④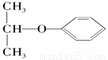 属于醚
属于醚
A.①② B.②③ C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
银器的保护主要是维持它的原貌,对于轻微腐蚀蒙有硫化银的银器,可将其和铝片接触一起浸泡在稀NaOH溶液中,经一定时间污迹消失,取出后用水洗干净,再用软布或棉团擦光。有关叙述不正确的是
A.溶液中的OH-向负极移动
B.在银表面上的反应为:Ag2S+2e-=2Ag+S2-
C.在铝表面的反应为:Al-3e-=Al3+
D.在铝表面的反应为:Al+4OH--3e-=AlO2-+2H2O
查看答案和解析>>
科目:高中化学 来源:2016届江西师大附中、临川一中高三上第一次联考化学试卷(解析版) 题型:填空题
N2H4(联氨又称肼)一种无色发烟的、具有腐蚀性和强还原性的无色油状液体,它是一种重要的化工试剂,在生产和生活中有着重要的作用。
(1)推测有关N2H4的性质,下列说法正确的是
A.具有高度吸湿性、可燃性
B.有微弱的氨味,与甲醇,乙醇互溶,但不溶于乙醚、氯仿和苯
C.N2H4的水溶液呈弱碱性,
D.联氨的水溶液既有氧化性又有还原性,酸性溶液以氧化性为主,还原产物是N2,碱性溶液以还原性为主,氧化产物是NH4+
E.高温加热时分解为氮气、氢气和氨气。
(2)请写出N2H5+的电子式:__________________________
(3)在高锰酸钾催化剂存在下,尿素(CO(NH2)2)和次氯酸钠-氢氧化钠溶液反应制得联氨,它和水能按任意比例互相混溶,形成稳定的水合肼N2H4·H2O写出反应的离子方程式:______________________
(4)发射卫星可用肼为燃料,用NO2作氧化剂,二者发生反应生成氮气和水蒸气。已知:
N2(g)+2O2(g)=2NO2 (g) H=+67.7kJ•mol-1,N2H4(g)+O2(g)=N2(g)+2H2O(g) H=-534kJ•mol-1,
写出气态肼和NO2反应的热化学方程式__________。
(5)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,负极电极反应式是____________________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上学期12月月考化学试卷(解析版) 题型:选择题
在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是
A.Ca2+、Na+、NO3-、CO32- B.Mg2+、Cl-、NH4+、SO42-
C.K+、Cl-、HCO3-、NO3- D.Ca2+、Na+、Fe3+、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com