
| A. | 在0℃,101 kPa时,22.4 L氢气中含有NA个氢原子 | |
| B. | 在H2O2+Cl2═2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| D. | NA个一氧化碳分子和0.5mol甲烷的质量比为7:2 |
分析 A、求出氢气的物质的量,然后根据氢气为双原子分子来分析;
B、求出氧气的物质的量,然后根据在此反应中,氧元素的价态由-1价变为0价来分析;
C、CO和乙烯的摩尔质量均为28g/mol;
D、NA个CO的物质的量为1mol,求出1molCO和0.5mol甲烷的质量.
解答 解:A、标况下22.4L氢气的物质的量为1mol,而氢气为双原子分子,故含2NA个氢原子,故A错误;
B、32g氧气的物质的量为1mol,而在此反应中,氧元素的价态由-1价变为0价,故当生成1mol氧气时转移2NA个电子,故B正确;
C、标准状况下,分子数为NA的CO、C2H4混合气体的物质的量为1mol,体积约为22.4L,而CO和乙烯的摩尔质量均为28g/mol,故混合气体的质量为28g,故C正确;
D、NA个CO的物质的量为1mol,故1molCO的质量为28g,0.5mol甲烷的质量为8g,故两者的质量只比为7:2,故D正确.
故选A.
点评 本题考查了物质的量和阿伏伽德罗常数的有关计算,难度不大,掌握公式的运用和物质结构特点是解题关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
| A. | x=1.6 | |
| B. | 实验 1 在前 6min 的反应速率 v(SO2)=0.2mol•L-1•min-1 | |
| C. | T1、T2的关系:T1>T2 | |
| D. | K1、K2的关系:K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,名称是:3-甲基-1-丁炔.
,名称是:3-甲基-1-丁炔.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
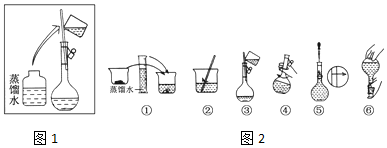
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
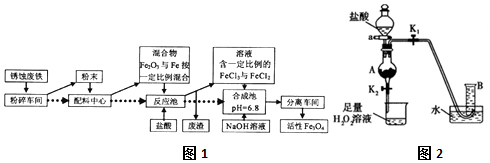
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可逆反应是指在同一条件下能同 时向正逆两个方向进行的反应 | |
| B. | 2HI$\stackrel{△}{?}$H2+I2是可逆反应 | |
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O与2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑互为可逆反应 | |
| D. | 只有可逆反应才存在化学平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| B. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe2+ | |
| C. | 电解熔融NaCl,阴极的电极反应式为:2Cl--2e-=Cl2↑ | |
| D. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com